Thromboprophylaxis in urological patients: to whom, how long, too much or too little?
DOI: 10.22591/magyurol.2018.4.molnara.156
Authors:
Molnár Ágnes dr., Villányi Kinga dr., Szántó Árpád dr.
Pécsi Tudományegyetem KK, Urológiai Klinika, Pécs (igazgató: Szántó Árpád dr.)
Summary
Due to the hypercoagulable state induced by surgery, serious complications of urological surgery include deep vein thrombosis and pulmonary embolism – together referred to as venous thromboembolism (VTE) – and major bleeding. Decisions regarding thromboprophylaxis using perioperative and postoperative low molecular weight heparin (LMWH) administration in urologic surgery involve a trade‐off between decreased risk of venous thromboembolism and increased risk of bleeding. Currently, there exists substantial practice variation in the use of thromboprophylaxis in urology, both within and between countries. This variation is unsurprising when one considers that recommendations from national and international guidelines often conflict. Consideration of LMWV administration, timing, dosage and duration are also a matter of debate in international literature. However, the majority of existing guidelines typically suggest thromboprophylaxis for most patients. Both patient‐ and procedure‐specific factors are critical in making an informed decision on the use of thromboprophylaxis.
Our aim is to summarize Guidelines proposal and to provide procedure and patient risk-specific guidance weighing the benefit of reduced VTE with the harm of increased bleeding.
LAPSZÁM: MAGYAR UROLÓGIA | 2018 | 30. ÉVFOLYAM, 4. SZÁM
Összefoglalás
Közismert, hogy minden műtéti beavatkozás két legrettegettebb szövődménye a tromboembólia és a vérzés. Az előbbi kivédésére évtizedek óta különböző heparinszármazékokat alkalmazunk, amelyek hatásuk révén a második szövődmény, a vérzés kockázatát növelik. A sebésznek a peri- és posztoperatív alacsony molekulasúlyú heparin (LMWH) kezelés alkalmazásakor egy igen keskeny mezsgyén belül kell egyensúlyoznia a kívánt védelem elérése és a vérzéses szövődmények elkerülésének érdekében. Az, hogy kinek, mikor és mennyi véralvadásgátló szert adjunk, a nemzetközi irodalomban is vita tárgyát képzi. Különböző szakmák és országok irányelvei valamint a különböző készítmények gyártóinak alkalmazási előiratai gyakran ellentétes ajánlásokat tesznek. Abban azonban mindenki egyetért, hogy trombózis profilaxis kell. Minden eset más, egyedi mérlegelést igényel, de felmerül a kérdés, általában melyik betegcsoportnak, mikor és mennyit adjunk.
Célunk az, hogy összefoglaljuk a konzervatív és operatív szakmák által javasolt irányelveket bemutatva ezzel egy betegcsoportra adaptált mintát a szerek biztonságos alkalmazása és a szövődmények csökkentése céljából.
Bevezetés
Az urológiai sebészeti beavatkozás során alkalmazott trombózis profilaxis előnyös és hátrányos következményei több tényezőtől függnek, ezeket beteg- és beavatkozás-specifikus tényezők közé sorolhatjuk. Az orvosoknak egy szűk terápiás mezsgyén belül kell egyensúlyozniuk a vénás tromboembóliás szövődmény (VTE) kivédése és a vérzéses szövődmények elkerülése érdekében. Az irodalomban számos randomizált vizsgálat zajlott különböző alacsony molekulasúlyú heparinok (low molecular weight heparin – LMWH) hatásának összehasonlítására, amelyek alapján az LMWH-k alkalmazása esetén a hasi- és kismedencei műtéten átesett betegeknél 50%-kal csökkent a VTE előfordulása, azonban a jelentős posztoperatív vérzés előfordulása is 50%-kal növekedett (1).
Azoknál a betegeknél, akiknél VTE kockázata magas és a vérzés szövődményeké alacsony, jelentősen profitálnak a profilaxis alkalmazásából. Ennél a betegcsoportnál az 50%-os vérzéses szövődményráta minimális veszélyt jelent. Azon betegcsoportnál viszont, akiknél az antikoaguláció nélküli tromboembóliás rizikó alacsony és a vérzésveszély igen magas, az ellenkezője igaz.
Igen kevés vizsgálat történt viszont a trombózis kockázatának felmérésére, az egyes beavatkozások során profilaxis alkalmazása, így a VTE-profilaxis pontos alkalmazására nincs egyértelmű irányelv. Így nem meglepő, hogy a különböző országokban alkalmazott gyakorlat jelentősen eltér egymástól. Nemzetközi viszonylatban a nemzeti urológus társaságok honlapjain és kiadványaiban több mint 160 ajánlás található (2).
Összefoglalónk célja, hogy az elérhető szakmai irányelvek alapján egy beteg- és beavatkozás-specifikus mintát mutassunk be a profilaxis biztonságos alkalmazása és a szövődmények csökkentése céljából.
American Urological Association (AUA) ajánlás
Az AUA Practice Guideline Comittee 2011-ben módosította 2009-ben kiadott ajánlásait (3). Ez a betegeket 4 rizikócsoportba sorolja (alacsony, közepes, magas és igen magas) az életkor, a rizikófaktorok jelenléte Greets és munkatársai által alkotott definíciók és a beavatkozás típusa („minor” és „major” beavatkozás) alapján (4). A minor beavatkozásokhoz a rövid műtéti idejű gyors felépülésű műtéteket sorolja, míg a major műtétekhez az összes minor csoportba nem sorolható. Ez a séma elsősorban a beteg rizikója alapján tesz javaslatot (1. táblázat).

Javaslatuk alapján az alábbi állapotok jelenléte esetén kell számolni magasabb vénás tromboembóliás rizikóval: nagyobb alsó végtagi trauma, immobilitás, malignitás, nem sebészi daganatterápia, korábbi mélyvénás trombózis, idősebb kor, terhesség, ösztrogéntartalmú antikoncipiens és hormonpótló kezelés, légzési- és keringési elégtelenség, gyulladásos bélbetegség, nephrosis szindróma, mieloproliferatív betegség, paroxizmális nocturnalis haemoglobinuria, obezitás, dohányzás, varicositás, centrál vénás kanül jelenléte, örökölt és szerzett trombofília. Arról, hogy ezen faktorok mennyire befolyásolják a VTE kialakulását, a társaság nem nyilatkozott. A profilaxis adásának időtartamára sem tesz pontos javaslatot, általánosságban a kórházi tartózkodás idejére terjed ki, és véleményük alapján az elbocsátás után csak az igen magas rizikójú betegeknél szükséges enoxaparin vagy warfarin alkalmazása.
Az AUA a fentiek mellett a beavatkozás módja szerint is megkülönbözteti az LMWH-profilaxis szükségességét. Ajánlásuk alapján általában a transzurethrális beavatkozások túlnyomó többségénél nincs szükség farmakológiai vagy mechanikai profilaxisra. A VTE és a vérzéses szövődmények igen változó mértékűek e betegek között, így a prosztata transzurethrális reszekciója után alkalmazott profilaxist személyre szabottan kell alkalmazni. Az anitiinkontinens beavatkozások és a kismedencei rekonstrukciós sebészeti műtétek is változó vérzéses és tromboembóliás rizikóval járnak, így ezeknél a beavatkozásoknál sem tesz egyértelmű ajánlásokat. Az igen korai mobilizációval járó periurethralis és sling műtéteknél nincs szükség profilaxisra. Ezzel ellentétben a vaginális, paravaginális rekonstrukciós, szuszpenziós műtétek és sacrocolpopexia magas VTE-rizikóval járnak, így ezeknél a beavatkozásoknál ajánlott a profilaxis alkalmazása.
A laparoszkópos és robottal végzett radikális műtétek tekintetében a társaság csak a prostatectomia, illetve nephrectomia tekintetében tesz ajánlásokat. Javasolják pneumatikus kompressziós készülék alkalmazását kiegészítve gyógyszeres profilaxissal a magas és igen magas rizikójú betegek esetében. A nyitott radikális műtétek esetében, különösen a prostatectomia és cystectomia esetében a társaság egyértelmű javaslata a mechanikai profilaxis alkalmazása, emellett mérlegelendő a farmakológiai profilaxissal való kiegészítés.
European Association of Urology (EAU) ajánlás
Az EAU a többi társasághoz hasonlóan 2016-ban közölte ajánlásait a tromboprofilaxis témakörében (5). Az ajánlások beavatkozás- és betegkockázat-specifikus rizikófaktorok figyelembevételével történtek. A szövődményeket nem halálos (szimptomatikus mélyvénás trombózis és pulmonalis embólia) és halálos tromboembóliás valamint nem halálos (reoperációt vagy intervenciót igénylő vérzés) és halálos vérzéses kategóriába sorolják, és felmérik ezek kockázatát. Az evidenciák alapján a súlyos vérzés kumulatív rizikója a beavatkozást követő reggelig 90%, míg az első 24 órában 50%. Ezzel szemben a vénás tromboembóliás szövődmények előfordulásának aránya az első 4 hétben konstans. Ez alapján a társaság a posztoperatív LMWH-kezelés indításának ideális időpontját a műtétet követő 24 óra múlva javasolja. Több randomizált vizsgálat metaanalízise azt igazolta, hogy a mechanikai profilaxis szintén 50%-kal csökkenti a VTE előfordulását, míg a posztoperatív vérzés lehetőségét nem növelik, azonban az ajánlás evidenciaszintje igen alacsony.
Az EAU által javasolt VTE betegadaptált rizikócsoportokat a 2. táblázat foglalja össze.
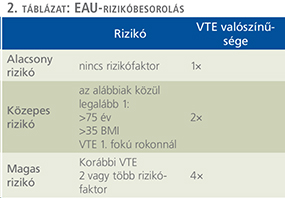
Az európai társaság a fent leírtakat figyelembe véve szigorú ajánlásokat tett a különböző műtéttípusok esetén alkalmazott profilaxist illetően. A kis, ambulánsan is elvégezhető beavatkozások esetében mind a gyógyszeres, mind a mechanikai profilaxis használata szükségtelen, mivel ezen betegek VTE kockázata az átlagpopulációéval azonos magas vérzéses rizikó mellett.
Radikális cystectomia esetében, függetlenül a végrehajtás módjától ajánlja mind a gyógyszeres, mind a mechanikai profilaxis alkalmazását.
A radikális prostatectomiák esetében ezzel szemben különbséget tesz a műtét módja és az elvégzett kismedencei lymphadenectomia mértékétől függően. A nyílt beavatkozások esetében mindig kell a betegnek gyógyszeres és mechanikai profilaxisban részesülnie. Robotasszisztált és laparoszkópos prostatectomia esetében a mechanikai profilaxis javasolt és csak lymphadenectomia elvégzése esetén ajánlott a gyógyszeres profilaxis alkalmazása.
Parciális nephrectomia esetében minden betegnél javasolt a mechanikai profilaxis. Nyílt beavatkozások esetén minden betegnél, míg laparoszkóppal végzett esetekben csak a magas tromboembóliás rizikójú betegeknél ajánlják LMWH alkalmazását. Radikális nephrectomia esetén hasonló ajánlásokat tettek. A trombectomiával járó esetekben viszont egyértelműen szükséges a mechanikai és farmakológiai profilaxis is, csakúgy, mint ureteronephrectomia, retroperitonealis lymphadenectomia esetén is.
A nem onkológiai indikációval végzett transzurethrális prosztatareszekció esetében egyértelműen a gyógyszeres profilaxis ellen foglalnak állást és mechanikai profilaxis alkalmazását is csak magas kockázatú betegeknél javasolják, hasonlóan a kismedencei rekonstrukciós, prolapsus és perkután kőműtétek esetében is.
National Insitute for Health and Care Excellence (NICE) – UK irányelv
Az angliai szervezet 2010-ben adta ki legfrissebb ajánlását a VTE megelőzésére mind a járóbeteg, mind az intézetben fekvő betegek számára (6). Az irányelveik a vérzés és a trombózisra való hajlam betegspecifikus és beavatkozás-specifikus rizikótényezőinek felderítésén alapulnak előre meghatározott „checklist” alapján. A NICE véleménye szerint a sebészeti beavatkozás előtt álló betegek mind magasabb rizikócsoportba tartoznak. A beavatkozás-specifikus rizikótényezőknek az alábbiakat találták:
- >90 perc teljes anesztéziai és műtéti idő,
- >60 perc műtéti idő a kismedencében vagy az alsó végtagokon, akut beavatkozás gyulladás vagy hasi történés esetén,
- immobilitást eredményező beavatkozások.
A betegspecifikus tényezőknek az alábbiakat határozták meg: aktív tumoros betegség, aktív tumorkezelés, >60 év, ITO-kezelés, dehidráció, ismert trombofília, BMI >30, egy vagy több szignifikáns komorbiditás, 1. fokú rokonnál VTE, hormonpótló kezelés, ösztrogéntartalmú antikoncopiens (OAC), varicositás phlebitisszel, terhesség, 6> posztpartum.
A NICE megállapít vérzésre hajalmosító tényezőket is, úgymint szerzett vérzészavarok (akut májelégtelenség), antikoaguláns kezelés (pl. warfarin), spinál anesztézia/lumbálpunkció/epidural anesztézia igény 4 órán belül vagy a következő 12 órában, akut stroke, thrombocytopenia, kontrollálatlan hipertónia (>230/120 Hgmm), kezeletlen örökölt vérzészavar.
A NICE javaslata alapján profilaxis szükséges minden olyan betegnek, aki magas kockázati csoportba sorolható. Az általuk javasolt profilaxis egyrészt mechanikai (kompressziós harisnya, intermittáló pneumatikus kompressziós készülék), a mobilizáció megkezdéséig kell folytatni, másrészt LMWH-profilaxis a teljes mobilizáció megkezdéséig, 5-7 napig. Onkológiai indikációval végzett hasi-kismedencei műtéten átesett betegek esetében ez 28 napra kiterjesztendő.
Magyar Thrombosis és Haemostasis Társaság, Transzfúziológiai és Hematológiai Szakmai Kollégium állásfoglalás
Az Egészségügyi Minisztérium 2011-ben publikálta a vénás tromboembóliák megelőzésére szóló irányelveit a belgyógyászati és sebészeti szakmák részére. Ennek alapja szintén a betegek és beavatkozások különböző kockázati csoportba való besorolása, amely a 3. táblázatban található (6, 7).

A betegspecifikus kockázati tényezők a nemzetközi irodalomnak megfelelően: trombofíliák, mieloproliferatív kórképek, paroxizmális nocturnalis haemoglobinuria, aktív hemolízis, nephrosis szindróma, malignus betegségek és azok kezelése során létrejött cytolisis, citosztatikus kezelés, korábbi VTE/AMI, antifoszfolipid szindróma, infekció, OAC, ösztrogénpótlás, terhesség és gyermekágy, tartós ágynyugalom, alsó végtag rögzítése és az ebből bekövetkező immobilitás, obesitas, varicositás, >6 h repülőút, dohányzás.
A javasolt profilaxis a kis kockázatú betegek esetében a korai mobilizálás, mechanikai profilaxis és a megfelelő folyadékpótlás. Ebben az ajánlásban a közepes, nagy és igen nagy kockázatú betegek profilaxisa között nincs különbség. Elektív műtétek esetén javasolt LMWH adása a műtét előtt 2 órával a gyógyszer alkalmazási előirat szerintit dózisban (ld. Függelék), amelyet igen nagy kockázatú betegek esetében a műtét befejezését követő 6 óra múlva ismételni kell, majd ezt követően naponta egy alkalommal szükséges folytatni. A kezelést a teljes mobilizációig, az igen nagy kockázatú betegek esetében 4 hétig folytatni kell. Emellett javasolja a megfelelő kompressziós grádienst biztosító elasztikus harisnya alkalmazását is. Ezen javaslatok azonban nem urológiai specifikusak, nem kerül többek között tárgyalásra az egyik leggyakrabban végzett műtéttípus, a prosztata transzurethrális reszekciója sem.
A preoperatív trombocitaaggregáció-gátló szerek és antikoaguláns kezelés menedzsmentje
Az elektív műtétek esetén a tromboembóliás és vérzéses szövődmények kivédése céljából szükséges a profilaxis helyes megválasztása. Számos beteg különböző kardiovaszkuláris és neurológiai állapot megelőzése céljából különféle antikoaguláns kezelésben részesül. Ezen gyógyszerek hatásának lecsengési ideje a gyógyszer elhagyása esetén is több nap. Azonban ezen betegek esetében alapvető fontosságú a véralvadásgátlás fenntartása, amely a beavatkozás során jelentős mértékben megemelné a vérzés kockázatát, így azok hatásának felfüggesztése szükséges. Az irodalomban is vitatott a különböző szakmák részéről, hogy melyik betegnek kell a korábbi per os antikoaguláns kezelését átállítani a sebészi beavatkozások előtt a gyógyszeresen könnyen felfüggeszthető, rövidebb hatásidővel rendelkező heparinokra vagy azok származékaira, mikor és milyen adagolásra. 2014-ben megjelent, kardiológusok és aneszteziológusok által publikált tanulmány alapján „áthidaló” („bridging”) kezelés csak magas trombózisrizikó és K-vitamin-antagonista kezelés együttes fennállása esetén szükséges (9). A különböző rizikócsoportokat a 4. táblázatban foglaljuk össze.
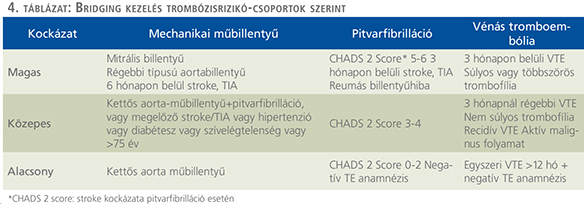
Az ajánlás alapján a K-vitamin-antagonista hatású gyógyszereket alacsony vérzéses rizikójú beavatkozások esetén nem szükséges elhagyni. Alacsony és közepes trombózisrizikó esetén elégséges a beavatkozás előtt 4-5 nappal ezen gyógyszerek szedését abbahagyni, áthidaló kezelést nem kell alkalmazni és a műtét előtt a véralvadási paramétereket ellenőrizni szükséges. Magas trombózisrizikójú betegek esetén korábbi warfarin terápiát a műtét előtti 5. napon kell felfüggeszteni és a 3. naptól kezdve terápiás dózisú LMWH-t indítani a műtétet megelőző 24 óráig. Acenokumarol (Syncumar) tartalmú készítmény szedése esetén azt a beavatkozás előtti 3. napon kell abbahagyni és a műtét előtt 48 órával kell terápiás dózisú LMWH-kezelést adni szintén a műtétet megelőző 24 óráig. Alacsony vérzéses rizikójú betegek esetében ezen szereket a posztoperatív első napon, míg magas rizikó esetén 48-72 órával később lehet legkorábban visszaállítani, addig a vérzés rizikójától függően profilaktikus vagy terápiás LMWH adása szükséges.
Az új típusú antikoaguláns szerek esetében az „áthidaló” LMWH-kezelés nem javasolt. A rivaroxaban, apixaban és edoxaban tartalmú készítmények esetén a beavatkozás előtt 3., míg a dabigatran tartalmú gyógyszerek esetén 4-5 nappal kell annak szedését felfüggeszteni. Alacsony vérzéses rizikójú műtét esetén ezen szerek a posztoperatív első nap visszaállíthatók, míg közepes és magas rizikó esetén 72 órás profilaktikus dózisú LMWH-kezelés szükséges az eredeti terápia visszaállítása esetén.
A trombocitaaggregáció-gátló szerek közül az aszpirin elhagyását csak magas vérzéses rizikó esetén ajánlják, ilyenkor javasolt azt a tervezett beavatkozás előtt 3 nappal felfüggeszteni. Gyógyszerkibocsátó koronáriastent esetén azonban még ilyen esetekben sem hagyható el.
A clopidogrel és ticagrelor tartalmú készítmények esetén 5 nap, míg plasugrel esetén 7 nap a műtét előtti javasolt gyógyszer-felfüggesztési időtartam. Ezen gyógyszereket javasolt minél hamarabb visszaállítani, ideálisan a bőrzárást követő 24 óra múlva.
Megbeszélés
Az irodalmat áttekintve az általunk trombózis profilaxis céljából alkalmazott terápiás elvek az alábbiak a beavatkozás specifikus tényezők figyelembe vételével:
- Scrotalis műtétek, kivéve tumoros szemikasztráció és absecdalt orhcidoepidimytis, varicocele, cirkumcízió, urethrotomia interna, hólyagnyaki sclerosis miatt végzett TURP, csak hólyagkőzúzás, meatotomia, húgycsőpolipus, szalagműtétek + fiatal életkor, rizikófaktorok nélkül: kompressziós harisnya, korai mobilizáció, hidráció.
- Tumoros szemikasztráció, TURB, trokár TURP, kismedencei rekonstrukciós műtétek, paravaginális műtétek, nem onkológiai nagyműtétek, vagy minor beavatkozások, de magas rizikóval: kompressziós harisnya a mobilizáció megkezdéséig + LMWH a teljes mobilizációig, de max. 7-10 napig.
- Infekció kezelése, illetve emiatt végzett műtét: LMWH az infekció zajlásának ideje alatt.
- Onkológiai műtétek, uroszepszis: kompressziós harisnya a mobilizáció megkezdéséig + LMWH 4 hétig.
A preoperatív profilaxis a kis kockázat kivételével a műtét előtt 12 órával történjen meg, igen magas rizikó esetén a műtét után 6 órával ismételve, 24 óra múlva napi 1×.
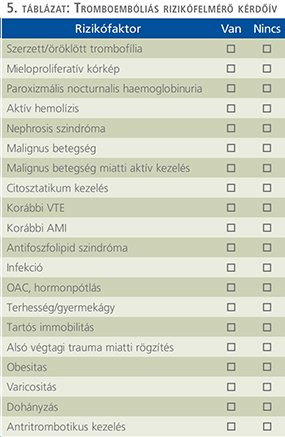
Emellett javasoljuk minden beteg felvételekor történő, a vénás tromboembóliás események betegspecifikus rizikófaktorainak felmérését minden betegnél (5. táblázat).
Az elmúlt években a trombózis profilaxis irányelveiben is jelentős változások jelentkeztek. Az új iránymutatások felállítása során a korábbi szakértők mellett a klinikai szakmák is bevonásra kerültek. Az új típusú antikoaguláns szerek megjelenésével háttérbe szorult a „bridging”, emellett a gyógyszerek eliminálásban fontos szerepet játszó vesefunkció adaptált dozírozás előtérbe került. Habár a heparinszármazékok a rövid hatástartam és a relatíve könnyű és olcsó felfüggeszthetőség miatt még mindig a perioperatív profilaxis elsőként választandó szerei, azonban az egyéb területeken történő alkalmazásuk háttérbe szorult. Ennek megfelelően az LMWH-gyártók piaci részesedése az elmúlt hat évben csaknem a felére csökkent. Ezek alapján felmerül az is, hogy kinek az érdeke a különböző heparinszármazékok nemritkán indokolatlanul hosszú ideig történő alkalmazása, a betegé esetlegesen a piacé?
FÜGGELÉK: kivonat az egyes készítmények alkalmazási előiratából
CLEXAN
Vénás tromboembóliás szövődmény megelőzésére közepes és magas kockázatú műtéti beavatkozás esetén
A tromboembóliás szövődmény kialakulásának kockázata egyénileg felbecsülhető validált, kockázatbesorolási modell alapján.
- A tromboembólia szempontjából közepes rizikójú betegeknek az enoxaparin-nátrium ajánlott adagja 2000 NE (20 mg) naponta egy alkalommal szubkután (sc.) injekció formájában. A sebészeti beavatkozás előtt (2 órával a műtétet megelőzően) beadott 2000 NE (20 mg) enoxaparin-nátrium hatásosnak és biztonságosnak bizonyult közepes kockázatú műtéti beavatkozás esetén.
A közepes kockázatú betegeknél az enoxaparin-nátrium-kezelés időtartama minimum 7-10 nap, függetlenült a klinikai állapot (pl. mobilitás) alakulásától. A profilaktikus kezelést mindaddig folytatni kell, amíg a beteg mobilitása jelentősen korlátozott.
- A tromboembólia szempontjából nagy rizikójú betegeknek az enoxaparin-nátrium ajánlott adagja 4000 NE (40 mg) naponta egy alkalommal szubkután (sc.) injekció formájában, amit lehetőleg a műtét előtt 12 órával kell elkezdeni. Amennyiben a műtét előtti 12 óránál korábban van szükség az enoxaparin-nátrium profilaktikus alkalmazására (pl. ortopéd sebészeti beavatkozásra váró magas rizikójú beteg esetében), az utolsó injekciót a műtét előtt legalább 12 órával kell beadni, és a kezelést a műtét után 12 órával kell folytatni.
- Nagyobb ortopéd sebészeti beavatkozáson áteső betegeknél kiterjesztett, legalább 5 hétig tartó tromboprofilaxis javasolt.
- Hasi vagy kismedencei daganat műtéti eltávolításán áteső, vénás tromboembólia (VTE) szempontjából nagy rizikójú betegeknek meghosszabbított, legalább 4 hétig tartó tromboprofilaxis javasolt.
Közepes és enyhe vesekárosodás
Túlsúlyos betegek esetében nagyobb a tromboembólia kialakulásának kockázata. A profilaktikus dózisok hatásosságát és biztonságosságát túlsúlyos betegek esetében (BMI >30 kg/m2) még nem határozták meg teljes mértékben, így a dózismódosításra vonatkozóan nincs megállapodás.
FRAXIPARIN
Tromboembóliás megbetegedések megelőzése
Naponta 1 alkalommal sc. injekcióban kell alkalmazni a készítményt.
Műtéti beavatkozások esetén
Általános érzéstelenítésben végzett sebészeti beavatkozások során alkalmazható az alábbiakban megadott adagolás.
Közepes kockázat (pl. általános sebészeti beavatkozás) esetén
Naponta 1-szer 0,3 ml (2850 anti-Xa NE) alkalmazandó sc. injekcióban.
2-4 órával a sebészeti beavatkozás előtt kell az első 0,3 ml-es (2850 anti-Xa NE) injekciót sc. beadni.
Ugyanezt a sc. adagot kell naponta 1-szer ismételni a kockázati időtartam alatt, a beteg mobilizációjának befejezéséig (de legalább 7 napon keresztül).
Magas kockázat (pl. ortopéd-sebészeti beavatkozás) esetén
Az adagot a beteg testtömege alapján kell meghatározni (38 anti-Xa NE/ttkg), és az így kiszámított dózist kell alkalmazni naponta 1-szer, sc. (lásd 1. táblázat):
- az első dózis beadása szubkután injekcióban 12 órával a műtét előtt,
- ezután ugyanennek a dózisnak a beadása 12 órával a műtét után történjen,
- majd naponta egyszer kell ismételni ugyanezt az adagot a 4. posztoperatív napig.
A 4. posztoperatív naptól nagyobb dózisokat (57 anti-Xa NE/ttkg) kell alkalmazni (lásd a táblázatot).
Súlyos vesekárosodásban szenvedő betegeknél (kreatinin-clearance <30 ml/perc) az adagot 25-33%-kal kell csökkenteni.
FRAGMIN
Pre-, peri- és posztoperatív vénás tromboembóliás szövődmények megelőzése
Szubkután injekció formájában általában naponta 1 alkalommal adandó.
Átlagos testsúly (50-100 ttkg) esetén:
- A tromboembólia mérsékelt kockázatával járó állapotokban: 2500 NE szubkután.
Például általános sebészetben: 2500 NE szubkután a műtét kezdetét megelőzően 1-2 órával.
A műtét után naponta egyszer – minden reggel – ugyancsak 2500 NE szubkután, amíg a beteg teljesen nem mobilizálható.
A tromboembólia fokozott kockázatával járó állapotaiban: 5000 NE szubkután
Például fokozott rizikóval járó általános sebészeti, onkológiai sebészeti, illetve ortopédiai műtéteknél:
- Preoperatívan 5000 NE szubkután a műtétet megelőző este, majd a műtétet követően naponta egyszer – minden este – ismételten 5000 NE szubkután adagolva, a beteg mobilizálhatóságának eléréséig – átlagosan 7-10 napig.
Alternatívaként adható az alábbi módon is: - Preoperatívan 2500 NE szubkután a műtétet megelőzően 1-2 órával, majd 8-12 órával, de a műtét végétől számítva legalább 4 órával később, ismételten 2500 NE szubkután. A műtét utáni napokon naponta egyszer – minden reggel – 5000 NE szubkután, a mobilizálhatóság eléréséig.
A profilaxis prolongációja megfontolandó fennálló rizikófaktorral rendelkező betegek esetében (pl. obesitas, alsó végtagi parézis, malignitás), vagy anamnézisben szereplő mélyvénás trombózis/tromboembólia mellett.
Klinikailag jelentős vesekárosodás esetén, (a szérum kreatininszint a normálérték háromszorosa fölé emelkedik) a dalteparin adagját aszerint kell módosítani, hogy fenntartható legyen az 1 NE/ml (0,5-1,5 NE/ml intervallumban) anti-Xa terápiás szint.
References
1. Gould MK, Garcia DA, Wren SM, et al. American college of chest physicians: prevention of VTE in nonorthopedic surgical patients: antithrombotic therapy and prevention of thrombosis, 9th ed: american college of chest physicians evidence‐ based clinical practice guidelines. Chest 2012; 141(Suppl 2): e227S–77S.
2. Violette PD, Cartwright R, Briel M, Tikkinen KA, Guyatt G. Guideline of guidelines: thromboprophylaxis for urological surgery. BJU Int 2016 Sep; 118(3): 351–8. doi: 10.1111/bju.13496. Epub 2016 Apr 29. https://doi.org/10.1111/bju.13496
3. Forrest JB, Clemens JQ, Finamore P, et al. American urological association: AUA best practice statement for the prevention of deep vein thrombosis in patients undergoing urologic surgery. J Urol 2009; 181: 1170–7. Reviewed and validity confirmed 2011
4. Geerts WH, Pineo GF, Heit JA, et al. Prevention of venous thromboembolism: the Seventh ACCP conference on antithrombotic and thrombolytic therapy. Chest 2004; 126(3 Suppl): 338S–400S. https://doi.org/10.1378/chest.126.3_suppl.338S
5. EAU Guidelines on Thromboprophylaxis in Urologycal Surgery 2018.
6. Treasure T, Hill J. NICE guidance on reducing the risk of venous thromboembolism in patients admitted to hospital. J R Soc Med 2010; 103: 210–2. https://doi.org/10.1258/jrsm.2010.100086
7. Az Egészségügyi Minisztérium szakmai irányelve, A thromboemboliák megelőzése és kezelése; A Magyar Thrombosis és Haemostasis Társaság, felkért szakértők, és a Transzfúziológiai és Hematológiai Szakmai Kollégium 2011.
8. Pfliegler Gy. A tromboemboliák kockázatának csökkentése és kezelése. Az Egészségügyi Minisztérium Szakmai Irányelve 2011.
9. Kristensen SD, Knuuti J, Saraste A, Anker S, Bøtker HE, De Hert S, et al. 2014 ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and management European. J Anaesthesiology 2014; 31: 517–573. https://doi.org/10.1097/EJA.0000000000000150
Leave a Reply
You must be logged in to post a comment.