Criteria of a standard and high-quality care of prostate cancer for long-term survival of patients in good quality of life
DOI: 10.22591/magyurol.2021.3.tenkep.104
Authors:
Tenke Péter dr.1, Bodoky György dr.2, Géczi Lajos dr.3, Mangel László dr.4, Maráz Anikó dr.5, Nyirády Péter dr.6, Polgár Csaba dr.7 Rózsa Péter8, Csizmadia Ádám8
Buzogány István dr.1, Markó Róbert dr.2, Kardos Lilla dr.2, Papp Éva dr.2,Dombovári Péter dr.1
1Péterfy Kórház-Rendelőintézet és Manninger Jenő Országos Traumatológiai Intézet, Urológiai Osztály, Budapest (osztályvezető: Buzogány István dr.)
2Affidea Magyarország Kft. – Péterfy Kórház-Rendelőintézet és Manninger Jenő Országos Traumatológiai Intézet, Budapest
Summary
Objective: Prostate cancer care is a complex challenge: besides medical challenges, individual and social burdens of the disease are also significant. The aim of our study is to give recommendations for different professional organizations and decision-makers to improve expectancy and quality of life of men suffering from prostate cancer.
Method: The analysis is based on four sources, which includes a literature review, the presentation of relevant public Hungarian data, in-depth expert interviews, interviews and round-table discussions of preliminary results.
Result: It is founded that a significant progress has been made in some areas in recent years, but further steps are needed to ensure a modern, standard, quality patient care that is accessible to all.
Conclusion: Our recommendations are in accordance with national and international guidelines and with Whitepaper on Prostate Cancer by European Association of Urology. We believe that this work could increase quality of care in prostate cancer.
LAPSZÁM: MAGYAR UROLÓGIA | 2021 | 33. ÉVFOLYAM, 3. SZÁM
Összefoglalás
Cél: A prosztatadaganatok ellátása komplex társadalmi feladat: az orvosszakmai kihívásokon túl jelentősek a betegség egyéni és össztársadalmi terhei is. Ezért tanulmányunk célja, hogy olyan ajánlásokat fogalmazzon meg az érintett szakmai szervezetek és a döntéshozók számára, amelyekkel tovább javítható a prosztatarákkal élő férfiak életkilátása és életminősége.
Módszertan: Elemzésünk módszertanilag négy forráson alapszik, amelynek része a problémakörrel foglalkozó szakirodalmak feltárása, a hazai publikus adatbázisokban elérhető releváns adatok bemutatása, számos szakértői mélyinterjú, valamint az előzetes eredmények megvitatása kerekasztal-megbeszéléseken.
Eredmény: Tanulmányunk fő megállapítása, hogy egyes részterületeken jelentős fejlődés történt az elmúlt években, ugyanakkor a minden beteg számára elérhető, modern, standard, minőségi betegellátás érdekében további lépések megtétele szükséges.
Következtetés: A kidolgozott javaslatok alapján, összhangban a hazai és nemzetközi szakmai iránymutatásokkal, valamint a European Association of Urology Whitepaper on Prostate Cancer tanulmányával, véleményünk szerint kijelölhetőek azok a beavatkozási pontok, amelyek hozzájárulhatnak a standard és magas minőségű betegellátáshoz és ezáltal a betegek jó életminőségben eltöltött, hosszú túléléséhez.
Vezetői összefoglaló
A prosztatarák a férfiak körében a harmadik leggyakoribb, a teljes populációban pedig a negyedik leggyakoribb daganattípus. A betegség elsősorban az 50 évesnél idősebb férfiakat érinti és a társadalom várható élettartamának növekedésével egyre gyakoribbá válik. A betegség prevalenciája hazánkban is növekszik, a prosztatarákkal élő férfiak száma már meghaladja a 20 ezer főt. A tanulmányban alkalmazott becslés alapján a betegség direkt és indirekt költségei elérhetik az 50 milliárd forintot.
A prosztatarák Magyarországon évente több mint 4500 férfinél kerül felismerésre, amellyel a hazai incidencia ugyan az európai átlag alatt van, de mortalitása azt jóval meghaladja (5, 6). Ennek egyik oka, hogy a prosztatarákot sok esetben már csak előrehaladott stádiumban diagnosztizálják.
A korai stádiumban felismert és szükség esetén idejében kezelt prosztatarák eredményesen gyógyítható, az 5 éves túlélés csaknem 100%, míg áttétes formában mindössze 28% (1). A prosztatarák korai felismerése ezért életet menthet és csökkentheti az egészségügyi rendszer prosztatarákkal kapcsolatos kiadásait is. Előrehaladott stádiumban a kezelés célja, hogy a beteg életét – akár évekkel – megfelelő életminőség mellett hosszabbítsuk meg. A magasabb rizikójú betegek életkilátásai is jelentősen javíthatók megfelelő utánkövetéssel, egyénre szabott terápiával, amely során a modern készítmények megfelelő szekvenciális alkalmazása alapvető.
Tanulmányunk célja, hogy olyan ajánlásokat fogalmazzon meg az érintett szakmai szervezetek és a döntéshozók számára, amelyekkel tovább javítható a prosztatarákkal élő férfiak életkilátása és életminősége. Ennek érdekében elemeztük a prosztatarák társadalmi-gazdasági hatásait, valamint a betegellátás jelenlegi helyzetét, annak kihívásait.
Elemzésünk módszertanilag négy forráson alapszik, amelynek része a problémakörrel foglalkozó szakirodalmak feltárása, a hazai publikus adatbázisokban elérhető releváns adatok bemutatása, számos szakértői mélyinterjú, valamint a munkaverzió részletes megvitatása.
Tanulmányunk fő megállapítása, hogy egyes részterületeken jelentős fejlődés történt az elmúlt években, ugyanakkor a minden beteg számára elérhető, modern, standard, minőségi betegellátás érdekében további lépések megtétele szükséges.
Ezen további lépesek közül kiemelendő, hogy jelenleg nem áll rendelkezésre a nemzetközi irányelvekkel összhangban lévő, szakmai konszenzuson alapuló, rendszeresen aktualizált prosztatarák-kezelési irányelv Magyarországon. Az országban nem teljesülnek teljes mértékben a korai felismerés követelményei, sajnálatos módon az opportunisztikus szűréseken nem vesznek részt a rizikócsoportokba tartozó férfiak, ami az alacsony prosztatarák-tudatosság mellett azt eredményezi, hogy a betegek egy részét csak előrehaladott, sokszor áttétes stádiumban fedezik fel, amikor az életkilátások már jelentősen rosszabbak. A betegirányítási rendszer, az onkoteamek kezelési folyamatba történő bevonása, a betegek utánkövetése nem egységes, így sok beteg nem kapja meg időben a számára legmegfelelőbb ellátást. A multidiszciplináris döntéshozatal feltételei nem minden ellátóhelyen adottak, számos ellátóhelyről több szakma is hiányzik (gyógytornász, pszichológus, dietetikus), így a betegek életminősége szempontjából is kritikus rehabilitáció és megfelelő palliatív ellátás nem elérhető minden beteg számára.
A tanulmány következtetései alapján, összhangban a hazai és nemzetközi szakmai iránymutatásokkal, valamint a European Association of Urology Whitepaper on Prostate Cancer tanulmányával, az alábbi javaslatok fogalmazhatók meg.
Javaslatok
Korai felismerés és egészségtudatosság
1. Korai felismerés
- Az opportunisztikus szűrés és a korai felismerés feltételrendszerének meghatározása a konszenzus meeting keretében, mivel korai stádiumban történő felfedezés esetén a prosztatarák eredményesebben gyógyítható.
- Be kell vonni a háziorvosokat a korai felismerés folyamatába, kiemelt figyelemmel a családi halmozódás tekintetében. Megfontolandó, hogy megfelelő edukáció után a PSA legyen finanszírozott már a háziorvosnál.
- A prosztatarák kezelési irányelvébe kerüljön beépítésre a korai felismerést szolgáló eszközrendszer.
2. Prosztatarák-tudatosság
- A „prosztatarák-tudatosság” növeléséhez folyamatos laikus edukációra, ismeretterjesztésre van szükség, hangsúlyozva a prosztatarák korai felfedezésének előnyeit.
- Támogatni kell azt, hogy az egyes betegszervezetek, civil szervezetek, az orvosszakmával összefogásban edukációs kampányokkal elérhessék az érintett populációt. Ennek érdekében a sokszor igen szerény anyagi forrásokkal rendelkező szervezeteket anyagilag is támogatni szükséges.
Ellátás és kezelés
3. Hazai irányelv
- A szakma alakítson ki a nemzetközi irányelvekre alapozott, rendszeresen frissülő uroonkológiai prosztatarák-kezelési irányelvet, amelyhez igazodva elkészíthető és frissíthető a hazai finanszírozási protokoll is.
4. Standard betegutak
- Magas minőségű, standardizált, integrált ellátást kell kialakítani, amely multidiszciplináris és betegközpontú. Ennek érdekében olyan betegirányítási rendszert, betegutakat kell kiépíteni, amelyek biztosítják, hogy valamennyi prosztatarákkal élő beteg időben, egységesen megkapja a prosztatarák-kezelési irányelvében meghatározott ellátást.
- A betegség ellátásában részt vevő valamennyi egészségügyi szakember tájékoztatása, képzése kritikus a betegutak betartása szempontjából.
- Az egységes betegút, a betegek megfelelő utánkövetése érdekében meg kell teremteni a betegkövetés feltételrendszerét és kötelező ellenőrzési pontok beépítése is javasolt.
5. Onkoteam
- Biztosítani kell, hogy az onkoteam minden beteg esetén összehívásra kerüljön, azon a beteg érdekeit megfelelő módon vegyék figyelembe. A beteg kezelése az onkoteam iránymutatásaival összhangban folyjon. Javasolt, hogy a hatóság ösztönzők beépítésével optimalizálja az onkoteam működését.
- Optimalizálni kell az onkoteamek működését annak érdekében, hogy a prosztatarák ellátásához szükséges onkoteam minden tagja részt vehessen a multidiszciplináris döntéshozatalban, és fel kell tárni azokat a problémákat (pl. szakemberek hiánya, leterheltsége), amelyek akadályozhatják ezt.
- A világjárvány után is rendszeresíteni kell az online onkoteamek lehetőségét. Regionális onkoteam létrehozása is megfontolandó.
6. Hozzáférés az innovatív, személyre szabott terápiákhoz
- Lehetővé kell tenni, hogy minden prosztatarákos beteg időben hozzáférjen a számára a mindenkori legtöbb előnyt nyújtó innovatív kezelési lehetőségekhez, személyre szabott terápiákhoz.
- Az egyedi méltányossági kérelem döntési idejét javasolt 30 napra rövidíteni. Ehhez szakmai részről biztosítani szükséges, hogy a beérkező kérelem minden szükséges adatot tartalmazzon.
Életminőség és túlélés
7. Rehabilitáció
- Nagyobb hangsúlyt kell kapnia a betegek rehabilitációjának, a minimumfeltételek között kell szerepelnie adott intézményben gyógytornász, dietetikus és pszichológus jelenlétének.
- A folyamatba be kell vonni a palliatív ellátásban jártas szakembereket (palliatív nővér), szociális munkásokat is.
8. Együttműködés a betegszervezetekkel
- A betegségterhek csökkentésében, betegedukációban a betegszervezetek is jelentős segítséget nyújthatnak a prosztatarákkal élő férfiaknak. Erősíteni, formalizálni kell a betegszervezetek együttműködését az ellátóhelyekkel, szakmai szervezetekkel, annak érdekében, hogy a szakorvosok leterheltsége ellenére a betegek hiteles információkhoz jussanak és aktív, elkötelezett részesei legyenek a kezelési folyamatnak.
- Fontos, hogy a betegek számára elérhetők legyenek az irányelvnek megfelelő, egységes, részletes betegtájékoztatók.
9. Eredményesség mérése
- Az EAU javaslatai alapján betegtapasztalatokon alapuló eredménymutatók segítségével fel kell mérni a különböző ellátások hatékonyságát, a betegek életminőségére gyakorolt hatásait.
- Betegelégedettségi kérdőívek szükségesek, amelyek visszajelzést biztosítanak az ellátás minőségéről.
Kutatás és innováció
10. Adat
- A meglévő adatbázisokat (Nemzeti Rákregiszter, EESZT) fejleszteni szükséges.
- A valós idejű elemzésekre forrást kell biztosítani, hogy transzparensen mérhetők legyenek a prosztatarákos betegek korai felismerésében, kezelésében elért eredmények.
11. Digitalizáció
- Fejleszteni kell a hazai orvostársadalom digitális képességeit annak érdekében, hogy tudásuk megfelelő legyen az új, modern és jórészt digitalizált megoldások használatához. Ehhez a továbbképzési rendszer átalakítása javasolt.
- Fejleszteni kell a diagnosztika digitalizációját, elősegítve a képalkotó és patológiai konzultációkat.
- Javasolt az uroradiológus-továbbképzés.
12. Telemedicina
- Fel kell térképezni a telemedicina lehetőségeit a prosztatarák-ellátás területén is, amely nagyban csökkentheti a szakemberek leterheltségét, valamint a valós idejű adatszolgáltatás javíthatja az ellátás minőségét is.
1. A prosztatadaganat társadalmi terhei
A betegség kiemelt társadalmi jelentőségét több tényező együttesen magyarázza. Egyrészről a prosztatadaganatok a felnőtt férfilakosság jelentős hányadát érintik: 60 évesnél idősebb férfiak közül minden 46. küzd a betegséggel.
Az újonnan diagnosztizált esetek pedig meghaladják a 4500 főt.
Másrészről a megbetegedés nagymértékben ronthatja a betegek életminőségét, és ezzel párhuzamosan nő az ellátórendszer igénybevételének gyakorisága is.
A betegséghez gyakorta társul a mozgás nehezítettsége (különösen előrehaladott stádiumban), szégyenérzet, amely könnyen társadalmi izolációhoz vezethet.
Harmadsorban a daganatban szenvedők kezelése jelentős direkt és indirekt költségekkel is jár, amely nemcsak a társadalombiztosításnak jelent kihívást, de gyakorta a betegek életében is komoly kiadásként jelenik meg. Ezzel párhuzamosan pedig a gyakoribb orvos-beteg találkozás jelentősen megnöveli az orvosok leterheltségét is.
A prosztatarák társadalmi jelentőségét egyszerre adják, tehát az orvosszakmai kihívások és a betegség egyéni (életminőség, mindennapi élet, munkaképesség, szociális élet, szexualitás, partner-család) és össztársadalmi szocio-ökonómiai következményei (betegség kulturális és társadalmi elfogadása).
1.1 A prosztatadaganatról
A prosztatarák jellemzően (70−80%-ban) a dülmirigy perifériás zónájában alakul ki. Világszerte az egyik leggyakoribb újonnan felismert daganatos megbetegedés, amely a társadalom várható élettartamának növekedésével egyre nagyobb számban kerül kórismézésre, mivel előfordulási valószínűsége a korral emelkedik (1). Jelen ismeretek szerint kockázati tényezők az életkor, az etnikai hovatartozás és a családi halmozódás (3).
A prosztatadaganat kezdetben sokáig tünetszegény marad, csak késői, előrehaladott, olykor áttétes stádiumban okoz leginkább panaszokat.
A tünetek két nagy csoportba sorolhatók. Egyrészt a szövetszaporulatból, tumortérfogat-növekedésből eredő obstruktív és irritatív tünetek, amelyek ráadásul nem specifikusak, hisz nagyon sok más urológiai betegségben is megjelenhetnek: gyakori és sürgető vizelési inger; vizelet visszatartásának nehézsége; gyakori éjszakai vizelés (irritatív tünetek), vizelet elakadása; nehéz vizelés; szakaszos vizelés; gyengült vizeletsugár; vizeletcsepegés; túlfolyásos vizeletvesztés (obstruktív tünetek).
Másrészt előrehaladott stádiumban a metasztázisok (áttétek) megjelenése okozhat tüneteket. A prosztatadaganat elsősorban a csontokba, a tüdőbe és a kismedencei nyirokcsomókba ad áttétet, leggyakoribb tünet a csontáttét okozta fájdalom (83).
Ha a betegséget korai stádiumban diagnosztizálják, úgy a prosztatarák prognózisa kedvezőbb, kórlefolyása lassú, a beteg hosszú évekig élhet megfelelő terápia és gondozás mellett.
Az újonnan diagnosztizált (de novo) esetek 5–30%-a áttétes a felismerés időpontjában a fejlettebb országokban, amely elmaradottabb régiókban 40–70% is lehet. A de novo áttétesen felismert betegek túlélése kedvezőtlenebb, mint a lokalizált betegséggel felismerteké (4).
1.2 A harmadik leggyakoribb daganatos megbetegedés férfiaknál
1.2.1 Incidencia
A betegség társadalmi jelentőségének egyik fontos mutatója az érintett betegkör nagysága. A GLOBOCAN 2020-as adatai alapján Magyarországon 2020-ban 6234 új eset volt, ami az összes új daganatos megbetegedés 9,3%-a, az összes férfi daganatos megbetegedésnek pedig a 18,5%-a (5).
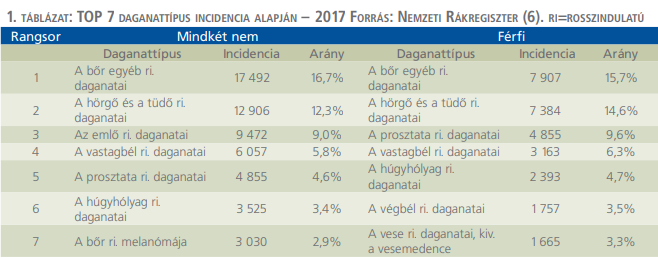
A Nemzeti Rákregiszter 2017-es adatai alapján a prosztatarák a férfiak körében a 3. leggyakoribb, míg a teljes populációban az 5. leggyakoribb daganattípus (1. táblázat).
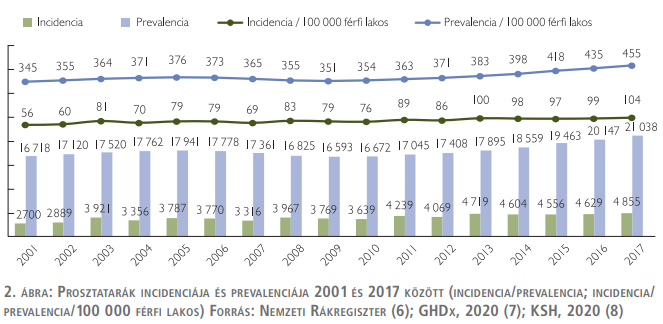
A Nemzeti Rákregiszter adatai alapján az incidencia növekvő trendet mutat: míg a 2000-es években az éves új esetszám 4000 fő alatt maradt, addig 2010 után rendre meghaladta azt, sőt 2013-ra 4500 fő fölé emelkedett.
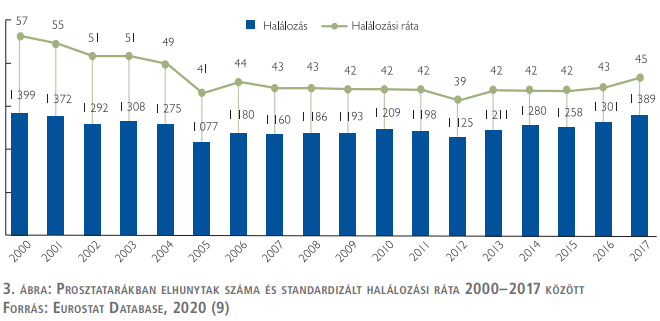
A férfilakosság körében tehát 100 000 főre minden évben 100 új prosztatarákos beteg jut (2. ábra).
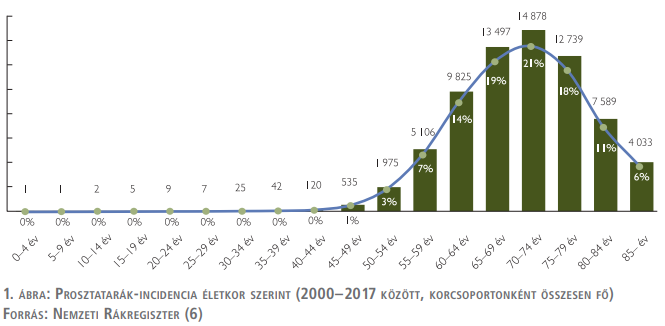
A prosztatarák incidenciája igen jelentős mértékben differenciálódik korcsoport szerint: a 0–44 éves korosztályban az éves új esetszám elenyésző, ugyanakkor 45 éves kor felett az incidencia jelentősen megugrik, és a 70–74 éves korosztálynál tetőzik (1. ábra) (6).
1.2.2 Prevalencia
A Global Health Data Exchange adatai alapján a 2017-es éves prevalencia 21 038 fő volt. Ez azt jelenti, hogy 100 000 lakosra 455 prosztatarákos beteg jutott (2. ábra).
A Global Health Data Exchange alapján a 2005–2009-es időszakot leszámítva folyamatosan nőtt a prosztatarákkal élő betegek száma, a magas incidenciához képest elenyésző az éves prevalencianövekedés: 4–4,5 ezer új beteg mellett a prevalencia csak kb. ezer fővel nő évente. Ez két okra vezethető vissza: egyrészről a betegség nagy számban érinti az idős, 65 év feletti korosztályt, ahol a prosztataráktól függetlenül is magas a mortalitás; másrészről magas a prosztatarák hazai mortalitása is (7) (2. ábra).
1.3 Mortalitás
A GLOBOCAN adatai alapján 2020-ban 1481-en haltak meg prosztatarákban, ezzel a betegség a 3. leggyakoribb halálok a férfiak esetében, és az 5. leggyakoribb daganatos halálok az összes daganatot tekintve nemtől függetlenül (2. táblázat).
A korábbiakban bemutatott egyre növekvő prosztatarák-incidencia és -prevalencia adatok ellenére az Eurostat adatai alapján a halálozás az elmúlt két évtizedben évi 1100–1500 fő között stagnált.

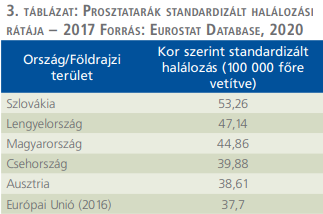
Az Eurostat adatai alapján a standardizált halálozási ráta 2000 és 2005 között csökkent, majd az elmúlt évtizedben 40–45 fő/100 000 lakos körül stagnált (3. táblázat és 3. ábra).
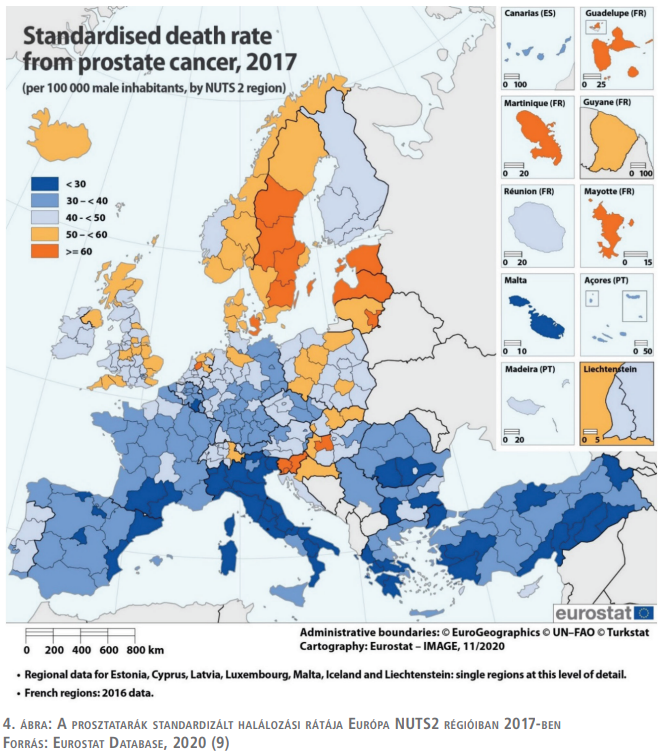
Összevetve az európai NUTS2 régiókat, kirívóan magas a prosztatarák mortalitása a Közép-Dunántúl régióban. Míg az Európai Unióban 37,7 volt a prosztatarák következtében
100 000 főre jutó standardhalálozás, addig a Közép-Dunántúlon 2017-ben 61,64, ami jóval meghaladja az országos 45-ös átlagot is (9) (4. ábra).
1.4 Gazdasági terhek
A prosztatarák növekvő incidenciája egyre nagyobb terhet ró az egészségügyre is. Rencz és munkatársai 2014-es tanulmányukban kísérletet tettek a prosztatarákkal kapcsolatos költségek felmérésére. Luengo-Fernandez és munkatársai 2009-es kutatására alapozva akkor úgy számoltak, hogy Magyarországon a daganatos betegségek gazdasági terhe a direkt és indirekt költségeket is figyelembe véve 320 milliárd forintot tett ki, amelyből 41 milliárd forint a prosztatarák terhe (10, 11).
A tanulmányban direkt költségként vették figyelembe az alapellátás, a járóbeteg-ellátás, a sürgősségi ellátás, a fekvőbeteg-ellátás és a gyógyszerek költségeit; míg indirekt költségként a mortalitás és morbiditás miatti termelékenységvesztést és az informális ellátás költségeit.
A prosztatarákkal kapcsolatos direkt és indirekt költségek összege 2019-es középárfolyamon számolva 41 milliárd forintnak felelne meg, ugyanakkor 2014 óta 25%-kal magasabb az incidencia, emellett számos új, magas költségű innovatív terápia és diagnosztikai módszer is befogadásra került. Becslésünk szerint így napjainkban a betegséggel kapcsolatos direkt és indirekt kiadások akár az 50 milliárd forintot is elérhetik. Ezekből 40%-ot, azaz 20 milliárd forintot jelentenek a direkt egészségügyi kiadások, míg 30 milliárd forintot az indirekt költségek.
1.4.1 Direkt egészségügyi költségek
Direkt egészségügyi költségek alá sorolandóak mindazon egészségügyi erőforrások költségei, amelyek közvetlenül szükségesek az egészségügyi beavatkozáshoz. Ide tartoznak többek között a megelőzéssel, a diagnosztikával, az ellátással, az ellátáshoz szükséges gyógyszerekkel, az ellátás során az esetleges adminisztrációval, az ellátást követő vagy kiegészítő szupportív ellátással, a mellékhatások kezelésével, illetve a rehabilitációval kapcsolatos költségek.
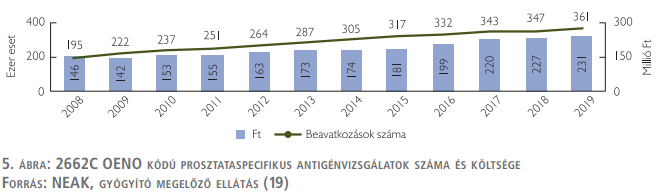
Egy korábbi NEAK adatelemzés szerint a prosztatarákhoz köthető direkt egészségügyi kiadások 2009 és 2013 között 8–12 milliárd forint között alakultak. Ezen összeg a CT- és MR-kiadásokat, a gyógyszerköltségeket, a fekvőbeteg-ellátás és a járóbeteg-ellátás költségeit foglalja magában. Az inflációval korrigálva a legutolsó 2013-as 8,5 milliárd forintos érték 2019-ben már 9,3 milliárd forintot jelentene. Ha a Rencz és munkatársai tanulmányából származó direkt és indirekt költségekre vonatkozó arányszámot elfogadjuk, akkor a NEAK adataiból kiindulva az indirekt költségekkel együtt 2019-ben 23,2 milliárd forintot tett ki a prosztatarák-ellátás teljes költsége.
2013-ra vonatkozóan elérhetők az egyes kasszák szerinti kiadások is, amely alapján megállapítható, hogy a prosztatadaganatokkal kapcsolatos kiadások döntően gyógyszervezéreltek (4. táblázat).
A teljes kiadás 60%-át fordították a prosztatadaganatok kezelésére szolgáló gyógyszerekre, ezt követték a fekvőbeteg- ellátás költségei (35%). Mivel az adatok 2013-ból állnak rendelkezésre, így joggal feltételezhető, hogy az új gyógyszeres lehetőségek közelmúltbeli befogadása még inkább a gyógyszerek felé tolta el a hangsúlyt.
1.4.2 Egyes innovatív terápiákra fordított kiadások nagysága
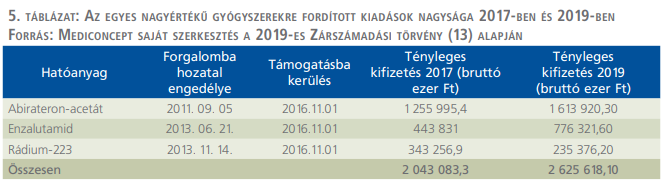
A 2019-es zárszámadási törvény alapján a 2016. november 1-jével befogadott egyes nagy értékű, innovatív szerekre több mint 2,6 milliárd forintot fordított a biztosító (5. táblázat).
A kiadások már az első teljes finanszírozott évben (2017) meghaladták a 2 milliárd forintot. Az abirateron-acetát esetén ez 28,5%-os, az enzalutamid esetén 75%-os növekedést, míg a rádium-223-diklorid esetében pedig 32%-os visszaesést jelent.
Ez a tendencia is jól szemlélteti, hogy jelentős igény mutatkozik a korszerű készítményekre, és hogy a folyamatos erőforrás-allokáció elengedhetetlen a területen.
1.4.3 Tipikus betegút éves költsége
A prosztatadaganat kezelésében az utóbbi évtized jelentős fejlődést eredményezett, a modern sugárterápia és az egyre hatékonyabb sebészi megoldások következtében a lokális betegség gyógyítási esélyei nőttek. Ennek ellenére jelentős azon betegek száma, akiknél a lokális ellátás ellenére progresszió alakul ki, vagy már a diagnózis felállításakor újonnan diagnosztizált (de novo) metasztatikus a betegségük.
A kezeléssel összefüggő költségek nagyban függenek attól, hogy a betegséget milyen stádiumban sikerül diagnosztizálni.
Szervre lokalizált közepes és magas kockázat esetén a költségek 350 ezer és 1,1 millió forint közé esnek, annak függvényében, hogy a betegen radikális prostatectomiát avagy sugárkezelést végeztek el, illetve hogy részesül-e ADT-kezelésben.
A metasztázissal rendelkező betegek esetén a választott innovatív terápia függvényében az éves terápiás költség 11,5–15,8 millió forint közé esik, amely szintén tartalmazza az egyéb orvosi költségeket is. Fontos ugyanakkor kiemelni, hogy a metasztázissal rendelkező betegek 5 éves várható túlélése mindössze 30%, ami jelentősen rosszabb a lokalizált betegségben szenvedő betegek által tapasztalt közel 100%-os 5 éves várható túléléshez viszonyítva.
1.4.4 Direkt egészségügyön kívüli költségek és indirekt költségek
Direkt, nem egészségügyi költségek alatt értendőek mindazon költségek, amelyek bár nem egészségügyi jellegű erőforrások igénybevételét takarják, de elengedhetetlenek az egészségügyi beavatkozás megvalósulásához.
Ezen költségek alá sorolható például a betegek egészségügyi szolgáltatások igénybevételéhez szükséges utazási és szállásköltségei, az otthonápolás költségei, a lakás esetleges, a beavatkozás által szükségessé vált átalakításának költségei vagy a speciális étrendek költségei (14).
Közvetett vagy indirekt költségek azok a költségek, amelyek nem feltétlenül az egészségügyi szolgáltatás igénybevételéből erednek, hanem a betegek életkörülményeinek a betegségből fakadó megváltozásából.
Ilyen változás lehet az, ha betegségük miatt kiesnek a munkából (legyen az akár fizetett, akár nem fizetett), ezáltal kevesebb jövedelmet termelnek. A munkából való kiesés költsége a beteg adott időszakra vonatkozó szuperbruttó jövedelme (15).
A szakirodalmi áttekintés nem talált releváns hazai kutatást a témakörben, de több nemzetközi tanulmány jelentős indirekt költségeket azonosít. Jayadevappa és munkatársai 3 hónappal a radikális prostatectomia után 5576 dolláros kiadásról számoltak be egy, az Amerikai Egyesült Államokban 2002 és 2005 között 597 főn végzett felmérésük alapján.
Az 5576 dollárból a direkt nem egészségügyi kiadások (utazási költségek, étkezés stb.) 649 dollárt (11,6%) tettek ki. Amennyiben számszerűsítésre kerül az utazásra fordított idő, a kísérők ideje, valamint a munkából való kiesés okozta időveszteség is további 4795 (86%) dollárt jelent (16).
Jól látható tehát, hogy a biztosító(k) által térített költségeken túl a betegek is jelentős kiadással szembesülnek, amelynek közel 90%-a valamely indirekt költségelemhez társítható.
2. A korai felismerés fontossága
2.1 Diagnosztikai eszközök
A prosztatarák diagnosztizálására számos eszközt használnak a világban, amelyek jelentős része hazánkban is elérhető. E fejezetben azon diagnosztikai lehetőségeket vesszük sorra, amelyek elengedhetetlenek a prosztatarák felismeréséhez és a betegség diagnózisának felállításához.
2.1.1 Prosztataspecifikus antigén vizsgálata
A prosztataspecifikus antigén (PSA) egy olyan fehérje, amelyet a szervezetben csak a prosztataszövet termel, az ondó alkotóelemeként az ejaculatum elfolyósodását segíti elő, ezáltal a megtermékenyítőképességben fontos szerepet tölt be. Kiválasztódását androgének szabályozzák, pubertáskortól kezdődően kimutatható egészséges férfiaknál is.
A PSA meghatározása a vérben alapvető a daganat felfedezésében. A PSA-vizsgálatnak nagy a szenzitivitása, azaz az emelkedés nagy érzékenységgel mutatható ki a prosztatadaganat korai stádiumában is. Azonban korlátozza az alkalmazhatóságát, hogy alacsony a specificitása, vagyis emelkedett PSA nem csak prosztatadaganat esetén fordul elő. Daganatok esetében csak nagyon ritkán fordul elő, hogy a PSA-szint nem emelkedik meg (5–8%). Egyértelmű küszöbérték nem határozható meg, de kiindulásként a 4 ng/ml érték az általánosan elfogadott.
A PSA értéke a kor előrehaladtával és a prosztata megnagyobbodásával növekszik. Az életkor miatt a határérték meghatározásánál korspecifikus küszöbértéket veszik figyelembe, illetve a prosztataméret befolyásoló hatásának kiküszöbölésére a PSA-denzitást alkalmazzák, amely a PSA-érték és a prosztatavolumen hányadosa.
Fontos figyelembe venni a PSA-változás dinamikáját is. A PSA-változás PSA-velocitással (időegység alatti változás) vagy a PSA-kettőződési idővel jellemezhető (PSADT).
- PSA-velocitás (PSAV), a szérum-PSA egy év alatt bekövetkezett abszolút növekedését jelenti, PSA (ng/ml/ év). Normál esetben maximum: 0,75 ng/ml/év.
- PSA doubling time (PSADT), a szérum-PSA exponenciális növekedését jelenti az időben, ezzel jellemezve a változást.
A PSA tehát a prosztatadaganatot jól jellemző tumormarker, azonban értékét mindig egyénileg kell értékelni (17, 18).
A PSA-tesztelés önmagában nem elégséges a prosztatarák diagnózisának felállításához, így minden esetben szükséges további vizsgálatok elvégzése, mint az MRI, majd pedig a biopszia és az azt követő szövettani vizsgálat.
PSA-tesztelést 2012 óta háziorvos nem végezhet.
A szakma javaslatára megfelelő felkészítés mellett vissza kell adni ezt a kompetenciát a háziorvosok számára.
2.1.2 Rectalis digitális vizsgálat
Mivel a legtöbb prosztatakarcinóma a perifériás zónából indul ki, ezért jól tapintható rectalis digitális vizsgálat (RDV) során. Az RDV során vizsgálható a prosztata mérete, konzisztenciája, felszíne, érzékenysége, környezethez való fixáltsága. Sajnos az RDV szenzitivitása alacsony, csak 40% körüli, viszont specificitása magas, meghaladja a 80%-ot.
A prosztatarákos betegek hozzávetőlegesen 18%-át a gyanús tapintási lelet alapján fedezik fel a PSA-értéktől függetlenül.
Az RDV és a PSA-tesztelés együttes alkalmazásával a korai felismerés eredményessége nagymértékben növelhető (2, 17, 18).
2.1.3 Képalkotó vizsgálatok
Standard képalkotó vizsgálat a transrectalis ultrahang (TRUS), amely azonban önmagában nem alkalmas a prosztatadaganat diagnosztizálására. Bár szenzitivitása megfelelő, azonban specificitása csekély, ezen felül nehezen reprodukálható, a vizsgálatot végző személye befolyásolhatja az eredményt. Mégis alapvető vizsgálati eszköz, mert a biopszia standardmódon ultrahangvezérelten, a végbél felől történik (3, 18, 20).
A multiparametrikus mágnesesrezonancia-vizsgálatok (mpMRI) elterjedése paradigmaváltást jelentett a lokalizált prosztatarák diagnosztizálásában. Az eszköz segít a felesleges biopsziák elkerülésében, illetve a daganatgyanús területek azonosításában – megjegyzendő ugyanakkor, hogy a prosztatarák igazolása csak szövettani mintavétel útján lehetséges, így gyanú esetén elkerülhetetlen a biopszia. Az mpMRI segítségével ráadásul a prosztatarák jobban lokalizálható, mint a véletlenszerűen végzett biopsziával, így az mpMRI-vel alátámasztott biopszia során sokkal jobb minta vehető, mint anélkül. Az mpMRI 10%-kal szorította vissza az inszignifikáns prosztatarák diagnosztizálását és 30%-kal a szükségtelen biopsziák végzését.
Staging vizsgálatként előrehaladottabb stádiumnál a nyirokcsomó-érintettség, illetve esetleges távoli áttét felmérésében CT- és MR-vizsgálat elvégzése szükséges. Csontmetasztázis kimutatására széles körben használt vizsgálat a csontszcintigráfia, amelynek diagnosztikus értékét jelentősen befolyásolja a PSA-szint, a klinikai stádium és tumor grade. Tünetet mutató betegnél minden esetben elvégzendő (2).
2.1.4 Biopszia
A prosztata végbélen keresztül történő tapintása típusos esetben emelkedett PSA mellett megerősíti a diagnózist és a mintavétel (tűbiopszia) egyértelmű indikációja.
Típusos tapintási lelet és normális PSA esetén is javasolt a mintavétel.
Nem jellegzetes tapintás és mérsékelten emelkedett PSA esetén a prosztatakarcinóma antigén (PCA) meghatározása segíthet eldönteni a mintavétel szükségességét. Ha a PSA jelentősen emelkedett vagy a követés során határozottan emelkedik, a daganat valószínűsége nagy, mintavétel javasolt. Mindkét lebenyből legalább 6-6 mintavétel javasolt, valamint a daganatra gyanús területekről külön. Ezzel együtt a negatív biopszia sem zárja ki egyértelműen a daganatot, így a beteg gondos követése, szükség esetén ismételt mintavétel javasolt.
Jelenleg egyedül a prosztatabiopszia, illetve az azt követő szövettani vizsgálat alkalmas prosztatarák igazolására (2).
A transrectalis ultrahangvizsgálat nem megfelelő módja a prosztatarák kimutatásának, ugyanakkor remek segítséget nyújt az ultrahangvezérelt biopszia elvégzéséhez. Az utóbbi időben az ultrahang mellett MRI-vezérlést is alkalmaznak (fúziós biopszia) annak érdekében, hogy a biopsziát a legmegfelelőbb területeken végezzék el. A biopsziát a fertőzésveszély elkerülése érdekében antibiotikum-védelemben végzik (18, 20).
2.2 Patológia és stádiumbesorolás
A prosztatarák leggyakrabban a prosztata-mirigyhámból kiinduló rosszindulatú daganat, szövettanilag adenocarcinoma. Leggyakrabban a prosztata perifériás zónájából indul ki (80–90%) és az esetek 50%-ában többgócú. A centrális előfordulás 10–20% (20).
A prosztatarák agresszivitásának értékeléséhez leggyakrabban az úgynevezett Gleason-pontszámot alkalmazzák. A Gleason-score egy szövettani mintában található két legjellemzőbb terület differenciáltsági fokának összege. A pontszám azt írja le, hogy az adott daganat mennyire tükrözi egészséges vagy abnormális szövet képét. A prosztatarák stádiumbesorolására klasszikusan a TNM-rendszer használatos világszerte.
Stádium szerinti incidenciaadat a tanulmány készültekor nem állt rendelkezésre Magyarországra vonatkozóan.
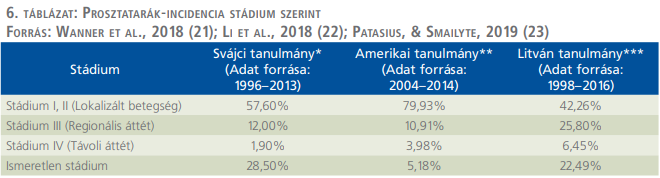
Nemzetközi adatokból kiolvasható, hogy a diagnózis megállapításakor a legtöbb beteg (40–80%) I., illetve II. stádiumban van, 11–26%-uk III. stádiumban, míg 2–6%-uk IV. stádiumú (6. táblázat).
Lokalizált stádiumban a betegség jelentősebb életminőség-romlás elkerülésével hatékonyan kezelhető, ugyanakkor regionális és távoli áttétek esetén jelentősen romlanak a betegek életkilátásai (4). A lokalizált stádiumban felismert betegek több mint 40%-a válik metasztatikussá a gyógyszeres vagy sebészi kasztráció és műtéti vagy sugárterápiás ellátás ellenére. Az újonnan diagnosztizált (de novo) esetek 5–30%-a áttétes a felismerés időpontjában a fejlettebb országokban, amely elmaradottabb régiókban 40–70% is lehet. A de novo áttétesen felismert betegek túlélése kedvezőtlenebb, mint a lokalizált betegséggel felismerteké.
2.3 Prosztatarák-tudatosság
A korai felismerés esélyét növelheti a férfiak prosztatarákkal kapcsolatos tájékozottsága, egészségtudatossága. Elsősorban ezen múlik, hogy egy férfi részt vesz-e opportunista szűrésen és kiderül-e a betegsége, vagy nem megy el és csak a tünetek jelentkezése után, kései stádiumban derül fény a prosztatarákra.
Az egészségtudatosság kapcsán két fontos problémát érdemes kiemelni:
- a férfiak prosztatarákkal kapcsolatos alulinformáltsága,
- elzárkózás a témától annak tabu jellege miatt.
Az egészségtudatos férfiak nyitottabbak a betegséggel kapcsolatos ismeretekre és sokszor önmaguk jelentkeznek prosztatarákszűrésekre. Jellemzően rendszeres testmozgást végeznek, figyelnek egészségükre, eljárnak orvoshoz, szűrésekre.
Sajnos többen vannak azok, akik kevésbé egészségtudatosak. A 35–64 éves magyar férfiak 31,1%-a naponta dohányzik. Sokan küzdenek súlyproblémával, az életkor emelkedésével nő a súlytöbblettel rendelkező férfiak aránya: a 65 évesek és annál idősebbek 77,6%-a túlsúlyos vagy elhízott (24). Figyelmeztető jel, hogy miközben a prosztatarák kialakulása az életkor előrehaladtával emelkedik, a 65 éves és annál idősebb magyar férfiak 39%-a még soha nem vett részt prosztatarákszűrésen (24) (6. ábra).
Szintén fontos probléma a prosztatarák stigmatizáló és a férfilétre kényes jellege. Az érintettek kevésbé hajlamosak beszélni tüneteikről, és nehezebben veszik rá magukat, hogy szakorvoshoz forduljanak problémájukkal.
Célként kell kitűzni, hogy a társadalom tagjai nyíltan beszéljenek a témáról, és tisztában legyenek a betegség korai felismerésének előnyeivel. Hangsúlyt kell fektetni a prosztatarák, mint tabu téma kezelésére is. Ebben segítség lehet olyan ismert emberek szerepvállalása, akik maguk is prosztatarákkal élnek.
A betegszervezeteknek kiemelt szerepe lehet abban, hogy üzeneteikkel a már diagnosztizált betegeken kívül az egészséges férfiakat és családtagjaikat is elérjék. A megfelelő hatékonyságú, egészségértést növelő kampányok megvalósításában szükséges a betegszervezeteket anyagilag is támogatni.
Fontos, hogy a betegek számára elérhetők legyenek az irányelvnek megfelelő részletes betegtájékoztatók.
2.4 Korai felismerés
A korai felismerés életet menthet, javítja az életminőség-mutatókat és csökkenti az egészségügyi rendszer prosztatarákkal kapcsolatos kiadásait.
A prosztatarák a betegség kezdeti stádiumában jól menedzselhető, a betegek többsége hosszú évekig teljes életet élhet.
A betegek túlélése és életminősége nagyban függ a betegség diagnóziskori stádiumától, ezért az egyik legfontosabb törekvés a minél korábbi felismerés.
Tanulmányunk egyik fontos megállapítása a korai felismeréssel és az ahhoz kapcsolódó szűrésekkel kapcsolatos szakmai dilemma: jelenleg nincs országos szűrőprogram, ugyanakkor a nemzetközi szakmai bizonyítékok alapján egy, minden 40 év feletti férfira kiterjesztett szűrés nem is feltétlen lenne indokolt. Ezért más, opportunista szűrésen alapuló megközelítés (kockázat alapú szűrés) megfontolása javasolt.
Egy átfogó, populációs alapú szűréssel bár több beteg lenne felfedezhető, ugyanakkor másik oldalról jellemzően túlkezelésekkel szembesülne az ellátórendszer. Ugyanis sok (alacsony és közepes rizikójú) beteg a diagnózis ellenére nem szorul aktív kezelésre, esetükben elegendő lenne a betegség aktív követése, folyamatos, rendszeres monitorozása. Az, hogy nem metasztatikus prosztatarák esetén a nem kezelés nem szükségszerűen hátrányosabb a beteg számára, mint a kezelés, tudományosan is alátámasztott: Wilt és munkatársai 2020-ban publikált tanulmányukban megmutatták, a folyamatos megfigyeléssel szemben a beavatkozás járhat életévnyereséggel, elsősorban a 65 évnél fiatalabb, mérsékelt kockázatú egészséges férfiak körében, ugyanakkor a beavatkozások az azzal járó funkcióvesztés és a szövődmények miatt nagyobb mértékben rontják az életminőséget, mint maga a betegséglefolyás (29). A betegek számára azonban a nem kezelés egy daganatos megbetegedés kapcsán joggal tűnik elfogadhatatlannak és emiatt vélhetően olyan esetekben is ragaszkodnának valamiféle kezeléshez, amikor annak nincs szakmai relevanciája. Ez a helyzet mindaddig megoldatlan marad, amíg nem áll rendelkezésre egy olyan technológia/stratégia, amellyel megnyugtatóan lehet orvosolni a túlkezelés kérdéskörét.
Jelenlegi ismereteink szerint tehát nem lehet teljesen megalapozottan egy általános országos szűrőprogram beindítása mellett érvelni. Ugyanakkor meg kell fontolni, hogy azonosíthatók-e olyan kockázati csoportok, ahol érdemes szervezett országos szűrőprogramot indítani.
Az ismert kockázati csoportok (pl. életkor és családi halmozódás) alapján való korai felismerésnek és az opportunista szűrésnek lehet relevanciája.
A kezelőorvosnak és a potenciális betegnek a következő ajánlásokat kell figyelembe vennie szűrés előtt és a korai megelőzéssel összefüggésben.
A különböző vizsgálatok alapján a prosztatarák genetikája komplexnek tűnik, és a betegség soktényezős etiológiája miatt egyelőre még nincs olyan genetikai vizsgálat, amely megfelelő bizonyossággal előre jelezné, hogy kik a leginkább veszélyeztetettek.

BRCA1- és BRCA2-gént hordozó családok vizsgálatával mutatták ki, hogy náluk nemcsak az emlőrák, hanem a prosztatarák rizikója is magasabb. A gént hordozó betegeknél a betegség fiatalabb korban manifesztálódik, és a kontrollcsoporthoz képest magasabb Gleason score-ral, ennek megfelelően a prognózisuk rosszabb, és így a várható túlélésük is rövidebb (8 vs. 4 év).
Elképzelhető, hogy egyéb faktorokkal együtt (PSA, rassz, életkor) már jobban meghatározható lesz az a csoport, akiknél van értelme a korai szűrővizsgálatoknak. Az ASCO ajánlása szerint például az ismerten magas genetikai kockázattal bíró betegeknél (pl. BRCA1-BRCA2) már 50 éves kor előtt érdemes elkezdeni a szűrést (25).
A korai felismerés második lépcsőjeként be kell építeni a kezelési irányelvbe annak eszközrendszerét, hogy minden ellátóhelyen világos legyen, mikor szükséges egy pácienst szűrni. Fontos, hogy felismerjék a betegek esetleges tüneteit és a jobban menedzselhető korai stádiumban meg is kaphassák a szükséges ellátást.
3. Kezelés és ellátás
3.1 Jelenlegi magyarországi kezelési gyakorlat
A prosztatarák standard kezelése lokalizált esetben műtét vagy sugárkezelés. Ezek (szükség esetén) gyógyszeres kezeléssel kombinálva lokálisan kiterjedt esetben is megkísérelhetők.
A nagyfokban lokálisan kiterjedt vagy áttétes betegség kezelésénél a vezető szerepet a gyógyszeres kezelés foglalja el. Ebben a stádiumban a kezelés célja palliatív, a betegség krónikus formában tartása, vagyis az élet hosszabbítása, megfelelő életminőség mellett akár évekig (20).
3.1.1 Kezelés
Magyarországon jelenleg nem áll rendelkezésre szakmai konszenzuson alapuló, aktualizált kezelési irányelv a prosztatarák ellátására vonatkozólag. Hazai kezelési irányelv híján a klinikusok a külföldi irányelvek (döntően az EAU és az NCCN iránymutatásai) felé fordulnak diagnosztikus és terápiás döntéseik meghozatalánál.
A nemzetközi guideline-ok rendszeresen frissülnek: az NCCN évente 4 kisebb-nagyobb karbantartást végez el iránymutatásán, az EAU pedig évi egyet.
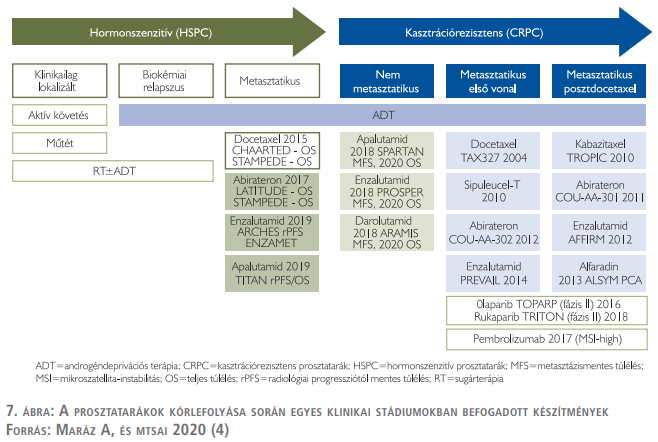
A hazánkban elérhető finanszírozási protokoll, amely nem minősül irányelvnek, 2016 után 2020 elején frissült utoljára és az alábbi kezelési lehetőségeket vonultatja fel lokalizált folyamat esetén:
- Aktív surveillance.
- Watchful-waiting.
- Radikális prostatectomia ± nyirokcsomó-eltávolítás (LA).
- Sugárterápia, amely lehet külső besugárzás vagy brachiterápia. A sugárkezelés kombinálható androgéndeprivációs terápiával.
- Sugárterápia, illetve radikális prostatectomia közötti választás kérdésében a rizikócsoport-meghatározásnak van alapvető szerepe (8. táblázat).
Az előrehaladott prosztatarák báziskezelése az androgéndeprivációs terápia (ADT).
Az ADT egy gyógyszerrel létrehozott kémiai kasztrációt jelent. Áttétes stádiumban a betegeknek a kedvezőbb eredményesség miatt elvileg életük végéig ADT-ben kell részesülniük.
Az androgéndeprivációs terápia gyógyszeres lehetőségei:
- gonadotropinfelszabadító hormon agonista vagy antagonista;
- teljes androgénblokád (TAB/CAB/MAB);
- időszakos ADT.
A betegség metasztatikussá válását követően a kezelés célja a tumor és a metasztázis növekedésének lassítása, a tünetek mérséklése.

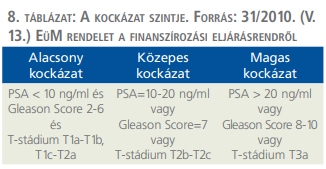
A kutatások eredményei azt mutatják, hogy a klinikailag agresszívebb lefolyású esetekben az ADT mellett alkalmazott kiegészítő kezelések (kemoterápia, új típusú hormonterápiák, célzott terápiák stb.) optimális alkalmazásával a magasabb rizikójú betegeknél is jelentősen javíthatók az életkilátások csupán annak a következtében, hogy megfelelően kerülnek időzítésre az egyes készítmények (7. ábra) (4).
A metasztatikus betegség eszköztára:
- kemoterápia
- hormonterápia (új típusú hormonális terápiák)
3.1.2 Betegút-menedzsment
„A klinikai betegút célja, hogy fejlessze az ellátás minőségét, csökkentse a kockázatokat, növelje a betegek elégedettségét, valamint az erőforrás-felhasználás hatékonyságát.” (De Bleser et al., 2006). A megkérdezett szakemberek szerint a betegútmenedzsment nem egységes az országban. Az ellátás minősége és sikere nagyban függ attól, hogy a beteget hol látják el, a kezelőorvos milyen szakmai ismeretekkel rendelkezik, hogy az onkoteam összehívásra került-e és az általuk javasolt terápiát követik-e, illetve hogy a beteg utánkövetése a szakmai ajánlások szerint zajlik-e.
A prosztatarák ellátásában részt vevő valamennyi szereplő számára fontos lenne a lehetőségekhez mérten standardizálni és konszenzuskonferencia keretein belül rögzíteni az ajánlott betegutakat. A megvalósításban elengedhetetlen lesz a prosztatarák-ellátás alsóbb szintjein dolgozó szakemberek megfelelő és folyamatos képzése és a betegedukáció.
3.1.2.1 Multidiszciplinaritás és az onkoteamek szerepe
A prosztatadaganatos betegek kezelése multidiszciplináris feladat. A csapat része az urológuson kívül a patológus, a radiológus, a sugárterápiás szakorvos, az onkológus, a gyógytornász és szükség szerint a pszichológus és a dietetikus is. Ideális esetben a beteg kezelésében részt vevő „team” a betegség felfedezését követően az onkológiai bizottsági ülésen beszéli át a kezelési lehetőségeket.
A betegek túlélésének emelése és az életminőségük javulásának érdekében kiemelten fontos, hogy összhangban az előírásokkal, az onkoteamek minden beteg esetében összehívásra kerüljenek.
Ennek garanciája lehet, ha a hatóság ösztönzők beépítésével optimalizálja az onkoteam működését Az onkoteam szerepét az 1/2012. (V. 31.) Emmi rendelet szabályozza. A rendelet szerint „A daganatos betegek ellátása komplex feladat, így a betegek optimális ellátásának meghatározása több szakterület orvosainak együttes feladata.” Ez ad garanciát arra, hogy a – nemzetközi ajánlások figyelembevételével – a betegek kivizsgálása és kezelése egységes legyen a daganatos betegek többszakmás ellátását végző onkológiai centrumokat működtető intézményeken belül, illetve országosan. Ennek alapján Magyarországon minden daganatos beteg klinikai adatait a diagnózis felállítását követően minél hamarabb, de legfeljebb 21 napon belül az onkoteam elé kell vinni. Ez az idő legfeljebb 30 napra meghosszabbítható (27).
Korai stádiumokban a sebész/urológus, a patológus és a sugárterapeuta intenzív kommunikációja elengedhetetlen a legjobb döntés meghozatalához. Ha ez a kommunikáció az onkoteam keretein belül valósul meg, az elősegíti a terápia mielőbbi megkezdését és lerövidíti a betegutakat.
Nagyon fontos, hogy az onkoteam-megbeszélés az elsődleges ellátás során megtörténjen, hiszen a beteg további sorsát, gyógyulási esélyét alapvetően a primer ellátás korszerűsége határozza meg.
A radikális prostatectomia és a sugárterápia egyaránt kuratív lehetőséget biztosít, ugyanakkor a beavatkozások jelentős hatással vannak a beteg életminőségére, így az onkoteam döntéseinél a beteg preferenciáit is figyelembe kell venni. Hasonlóan a watchful-waiting kérdésköréhez, amely esetében a beteg-
preferenciák szintén kiemelten fontosak.
A multidiszciplináris együttműködés kiemelten hangsúlyos a radiológus és az urológus között a biopszia megtervezésekor is, különösen, ha szükség és lehetőség van a biopsziát megelőző MRI-vizsgálat elvégzésére, mely nagyban hozzájárulhat a biopszia eredményességéhez. Ezt az eljárást nevezzük mpMRI által vezérelt fúziós biopsziának.
Restaging esetén, ha terápiaváltás válik szükségessé, szintén elengedhetetlen az onkoteam döntése.
Összességében a multidiszciplináris megközelítés előnye, hogy a több szakembert tömörítő onkoteam tagjai által a megfelelő információk megosztásával megnő az esély a beteg számára, hogy esetében a legmegfelelőbb terápia kerüljön kiválasztásra, ezáltal az elérhető legjobb életminőséget és túlélést biztosítva számára.
3.1.2.2 A betegek utánkövetése
A betegek utánkövetése elengedhetetlen eleme a prosztatarák kezelésének. Megfelelő utánkövetés híján a beteg a prosztatarák progressziója esetén nem kap időben ellátást, amelynek végzetes következményei lehetnek. Emiatt fontos az ellátási rendszerbe egy olyan jelzőrendszert beépíteni, amely az ellátás bármely szintjén dolgozó szakembereket figyelmezteti, ha az utánkövetett beteg vizsgálata esedékes.

Radikális prostatectomia és sugárterápia után az utánkövetés fontos eleme a PSA rendszeres (5 évig 5–12 havonta) ellenőrzése, amely, ha meghaladja a 2 ng/ml-es értéket, akkor az onkoteam összehívása indokolt a restaging megítélése érdekében.
A megfelelő utánkövetés egyik záloga az ellátás különböző szintjei közötti hatékony együttműködés.
4. Életminőség és túlélés
4.1 Betegségteher
A prosztatarák betegségterhe a betegségben töltött életévek (YLD) és a betegség miatt elvesztett életévek (YLL) alapján kerül bemutatásra (9. ábra).
A YLD azt mutatja meg, hogy egy egyén a neki prognosztizált életévekből mennyit tölt betegségben, míg a YLL azt mutatja meg, hogy várható éllettartamához képest mennyi életévet vesztett el a betegség miatt bekövetkezett korai halálozás következtében. Fontos mutató az egészségkárosodással korrigált életév (DALY) is, amely az YLD és az YLL összegeként kerül számszerűsítésre.
Magyarországon 2017-ben prosztatarák miatt 100 000 lakosra közel 40 betegségben töltött életév jutott, míg szintén
100 000 lakosra vetítve 416,65 életévveszteséget regisztrálhattunk. Így 2017-ben a prosztatarák betegségterhe mindösszesen 417 életév volt (9. ábra).
Az ábráról leolvasható, hogy 2007 után csökkent mind a DALY, mind az elveszített életévek száma, majd 2010-től újra növekedésnek indult 2014 (denosumab) és 2016 (abirateron, enzalutamid, Ra223) közé tehető a prosztatarák-ellátásban az első innovatív terápiák hazai támogatása, amelynek hatása az elveszített életévek csökkenő számában 2015 után meg is mutatkozott.
4.1.1 Betegségteher és életminőség korai stádiumban
A betegség korai stádiumban jól menedzselhető, lassú lefolyású. A betegek túlélése relatíve hosszú, így a betegségterhek a későbbi stádiumokhoz képest mérsékeltebbek.

4.1.2 Betegségteher és életminőség kései stádiumban
Kései stádiumban a betegség terhei növekednek, egyre nagyobb és gyakoribb terhet jelentve a beteg számára.
A prosztatarák lefolyása vagy maga a kezelés sok esetben a férfi nemzőképességének vagy erekciós képességének ideiglenes vagy akár végleges elvesztését hozhatja magával, amely jelentős pszichés megterhelést jelenthet a betegeknek.
A betegség progressziója (csontáttét megjelenése) és a kezelés okozta tünetek miatt a betegek gyakran inaktívak, amely további állapotromlást okoz. A túl sok pihenés az állóképesség, az izomerő és a mobilitás romlásához és elhízáshoz vezethet. A hormonkezelés prosztatarákban ezt a folyamatot különösen felgyorsítja, mellékhatásai lehetnek többek között: fáradtság, hőhullám, metabolikus szindróma, elhízás, libidócsökkenés, diabétesz fokozott kockázata, csontritkulás, patológiás csonttörések és fokozott kardiovaszkuláris rizikó (28).
A rehabilitáció mielőbbi megkezdése pszichológusok, gyógytornászok és dietetikusok bevonásával alapvető fontosságú, a beteg életminősége és túlélése szempontjából is. Ideális esetben a gyógytornászból, dietetikusból, pszichológusból, palliatív nővérből, szociális munkásból álló csapat a multidiszciplináris team integráns részeként a diagnózistól a kezelésen át a palliációig foglalkozik a betegekkel.
A prosztatarákkal élő férfiak esetében a mozgásnak, a szakember segítségével végzett gyógytornának fontos szerepe lehet a rehabilitációban, a kezeléssel kapcsolatos mellékhatások csökkentésében és az életminőség javításában.
A rendszeres mozgásnak a csont- és izomvesztés, illetve a fáradékonyság kivédésében van szerepe és a beteg túlélésére is jelentős befolyással van. Azoknál a prosztatarákos betegeknél, akik a diagnózist követően rendszeres, erőteljes mozgást végeznek (hetente 3 vagy több órát), szignifikánsan (50−60%-kal) alacsonyabb mind a betegségspecifikus, mind a teljes halálozás gyakorisága, ha azokkal a betegekkel hasonlítjuk össze őket, akik hetente 1 órát vagy kevesebbet mozognak.
Több mint 200, prosztataműtéten átesett férfinál prospektíven igazolták, hogy a kismedencei izmokat erősítő gyógytorna a műtét után egy évvel 51%-kal csökkentette az inkontinenciás epizódokat.
A rehabilitációnak ugyanakkor számos korlátja van: az ellátást végző intézményekben jelenleg nem minimum követelmény a dietetikus, a gyógytornász vagy a pszichológus megléte, így ezekre sokszor nincs is státusz. Rendelkezésre álló szakember nélkül pedig korlátozottak a rehabilitáció lehetőségei.
Ahhoz, hogy a betegterhek csökkenthetők legyenek, fontos objektíven ismerni azt, hogy a betegek számára mi és milyen mértékű terhet jelent. Emiatt megfontolandó az úgynevezett betegtapasztalatokon alapuló eredménymutatók (Patient Reported Outcomes – PROMs) használatával standardizált kérdőíves módszerrel felmérni a betegek terheit, így a különböző ellátások hatásai a betegek nézőpontjából is megismerhetővé válnának.
A betegségterhek csökkentésében a betegszervezetek is jelentős segítséget nyújthatnak a prosztatarákkal élő férfiaknak. Hidat képezhetnek a betegek és az ellátórendszer között, a rendelkezésre álló forrásaik terhére gyógytornász, pszichológus, dietetikus biztosításával a betegeknek számottevő segítséget nyújthatnak.
Abban is sokat tehetnek a betegszervezetek, hogy a prosztatarákkal élő férfiak is aktív részesei legyenek a saját kezelésüknek és maguk is tegyenek azért, hogy jobb életminőségben éljenek, hiszen a mellékhatások nagy része csökkenthető megfelelő életmóddal, rendszeres testmozgással és megfelelő diétával.
Ezért érdemes megfontolni a szakmai szervezetek, ellátóhelyek és a betegszervezetek közötti együttműködések erősítését, formalizálását is.
5. Kutatás és innováció
5.1 Az adatok elérhetősége és minősége
A prosztatarák-ellátás területén nagy hiányosság egy jól működő, átfogó, országos regiszter elérhetősége.
A regiszterből származó adatok értékes információkkal szolgálhatnának mind az ellátók, mind a kutatók, de a döntéshozók számára is a tendenciákról, a kezelések eredményességéről, a korai felismerés mértékéről stb. Az elemzések nyomán célzott programok készíthetők a beazonosított problémás területek javítására és a forrásokat hatékonyabban lehet allokálni.
Reális cél lehet a Nemzeti Rákregiszter továbbfejlesztése arra a szintre, hogy az adatokon big data elemzéseket lehessen végezni a prosztatarákkal kapcsolatban. Az adatszolgáltatók (ellátóhelyek) összeköttetése adott, azonban a közölt adatok jelenleg igen szerények, így első lépésként a regiszter által felhalmozott adatmennyiséget érdemes növelni. Fontos hangsúlyt fektetni az adatok minőségére, az adatbevitelt végző személyzet motivációjára.
Az EESZT elindulásával lehetőség nyílik a hatékonyabb adatgyűjtésre és adatelemzésre, ez azonban számos fejlesztést igényel. A rendszer alkalmas a leletek feltöltésére, azonban ehhez egységes leletezésre van szükség, ami a feldolgozást is egyszerűsítené.
Véleményünk szerint előremutató lenne a különböző adatbázisok összekapcsolása is.
Az erős evidenciákkal alátámasztott családi halmozódást, mint prosztatarák kockázati tényezőt, nem követi jelenleg adatbázis, így az érintett alanyok nem ismertek, számukra opportunista szűrés célzottan nem javasolható.
A következő években az orvoslásban egyre nagyobb szerepe lesz a molekuláris biológiának, míg informatikai részről a big data elemzésnek és felhasználásnak. A kettőt összefűzve olyan adatbázisok lesznek létrehozhatóak akár Magyarországon is, amelyek kiváló lehetőséget teremtenek az egyre inkább teret nyerő modern célzott terápiák alkalmazásának.
Az adatbázisok megfelelő szervezésének egyik kulcshozadéka az eredményesség mérése lehet, ami a legelőremutatóbb a kezelés minőségének javítása szempontjából.
5.2 A mesterséges intelligencia adta lehetőségek kihasználása
A big data következő lépcsőfokának tekinthető a mesterséges intelligencia és a különböző algoritmusok nagy adatbázisokon történő használata. Ezen eszközökkel gyorsítható az adatfeldolgozási folyamat és eredményeképp a valós időhöz közeli forrásallokáció és döntéstámogatás érhető el. Szerte a világban már számos kísérlet látható a mesterséges intelligencia diagnosztikában betölthető szerepére vonatkozóan, amely az idő előrehaladtával egyre inkább gyakorlattá válhat. Ilyen területek lehetnek az MRI-eredmények kiértékelése, illetve a staging vagy a kiinduló diagnosztikai eljárás támogatása.
5.3 Digitalizáció
Az orvostársadalom digitális képességeit fejleszteni szükséges, ezt követően pedig megfelelő rendszert kell kiépíteni az orvosok rendszeres digitális továbbképzésére.
A szoftveres követelmények lehetőséget teremtenének a diagnosztika digitalizációjára is. A diagnosztika területén ma már elérhetők olyan berendezések, amelyekkel az eddig mikroszkópon vizsgált minták digitalizálhatóak, és megfelelő felbontású monitorok segítségével elemezhetők. Ehhez azonban jelenleg hiányzik a hardveres háttér, szükség volna a minták szkennelésére szolgáló gépekre, és az azokat nagy felbontásban megjeleníteni képes monitorokra is. Ezen eszközök segítségével Magyarországon is kis beruházással elősegíthető lehet a diagnosztika digitalizációja, ezzel bővítve a távdiagnosztika lehetőségeit is.
5.4 A telemedicinában rejlő lehetőségek
Érdemes figyelemmel kísérni az olyan életminőség-javító megközelítések térnyerését is, mint a telemedicina.
A telemedicina révén az ellátást végző szakorvos az ellátás egy részét, mint a konzultációt, betegvezetést, laboratóriumi eredmények, illetve képalkotó vizsgálatok elemzését, receptírást, a beteg fizikai jelenléte nélkül is képes elvégezni.
A telemedicina elterjedésével olyan új szakmák is létrejöhetnek, mint az uroradiológus. A telemedicina hatására jelentősen javulhat a diagnosztika, jobban feltérképezhetővé válhat a kezelés minősége, így visszajelzés kapható az ellátásról.
Az onkoteam tagjainak is időt, energiát takaríthat meg a telemedicinális kommunikáció lehetősége.
6. A prosztatadaganatok hazai kezelési gyakorlatának általános értékelése
A prosztatarák ellátásával kapcsolatban számos kihívás sorolható fel, amelyeket a multidiszciplinaritás alapján kiválasztott 21 szakértővel folytatott mélyinterjú alapján állítottunk össze.
Az interjúalanyok előre definiált szempontrendszer mentén, egy 1-től 10-ig terjedő skálán értékelték a hazai prosztatarák-ellátást. Minél magasabb a pontérték, a szakértők annál inkább megvalósultnak látják az adott ellátási célokat a gyakorlatban.
Az interjúk alapján a legmagasabb érték 7,08, míg a legalacsonyabb 4,00 volt, azaz a szakemberek a hazai prosztatarák-ellátás több területén fejlesztést tartanak szükségesnek (10. ábra).
6.1 A hazai rendszer erősségei
Infrastrukturális háttér
A legmagasabb értékelést a megfelelő infrastrukturális háttér kapta (7,08). A megkérdezettek többsége beszámolt a közelmúltban történt jelentős infrastrukturális fejlesztésekről. Ennek köszönhetően sok helyen magas színvonalú környezetben zajlik a betegellátás. Ugyanakkor elhangzott, hogy ez a magas minőségű infrastruktúra leginkább csak a csúcsintézményekben érhető el, az MRI-hez és a PSMA PET/CT-hez való hozzáférés korlátozott.
Együttműködés
A második legmagasabb értéket (6,92) a betegellátásban kulcsszerepet játszó társszakmák, azaz az onkológusok, urológusok és sugárterapeuták együttműködése kapta.
A válaszadók szerint az urológus és onkológus szakorvosok, valamint sugárterapeuták között alapvetően jó a kapcsolat, munkájuk az onkoteamek tevékenységében is találkozik.
Finanszírozás
A finanszírozás kapcsán a szakemberek elmondták, hogy a legtöbb, prosztatarák-ellátáshoz szükséges terápia finanszírozott Magyarországon, ugyanakkor a legmodernebb terápiás eszközök – mint például a robotsebészet vagy a fúziós biopszia – még nem teljeskörűen érhető el az országban. Ezek, bár jelentős beruházást igényelnek, az ellátás minőségét szignifikánsan emelhetik.
Általánosságban megállapítható, hogy a rendszer eszközökkel való ellátottsága alapvetően elégséges, ugyanakkor technológiaváltásra van szükség ahhoz, hogy valóban a legmodernebb ellátás valósulhasson meg Magyarországon.
A terápiák hazai elérhetőségében folyamatosnak mondható a felzárkózás, ugyanakkor évek telhetnek el addig, míg egy, a világban már használatos innovatív terápia ténylegesen befogadásra kerül a hazai támogatási rendszerbe. Az innovatív készítmények bizonyos indikációkban kizárólag egyedi méltányossági kérelmek útján férhetőek csak hozzá. Itt jelentős akadály, hogy ezek elbírálása 60 nap is lehet. Fontosnak tartanák ezt az időt legalább 30 napra lerövidíteni. A kérelmek adminisztrációján az is rövidített, hogy a járvány óta online is beadhatók, amit érdemes lenne a későbbiekben is fenntartani.

6.2 A hazai prosztatarák-ellátás fejlesztésre szoruló területei
Standard, minőségi ellátás
A szakemberek véleménye szerint a magas minőségű ellátás nem érhető el valamennyi beteg számára, az elsősorban a jól felszerelt centrumokat jellemzi és azokat a kisebb ellátóhelyeket, ahol kiemelkedő szakember végzi az ellátásokat. Központi kérdésként merült fel az ellátások standardizálása. Az interjúalanyok beszámoltak róla, hogy sem az infrastruktúra, sem a szakembergárda képzettsége tekintetében nem beszélhetünk standard ellátásról. Úgy vélték, progresszivitás alapján további centralizációra volna szükség, miközben az alsóbb szintek edukációjára még nagyobb figyelmet fordítanak.
Jól szervezett betegutak
A megkérdezett szakemberek szerint a betegút-menedzsment nem egységes az országban. Az ellátás minősége és sikere nagyban függ attól, hogy a beteget hol látják el, a kezelőorvos milyen szakmai ismeretekkel rendelkezik, hogy az onkoteam időben, megfelelő összetételben összehívásra került-e és az általuk javasolt terápiát követik-e, illetve, hogy a beteg utánkövetése a szakmai ajánlások szerint zajlik-e. A szakemberek úgy látják, hogy az onkoteamek összehívását a finanszírozónak ösztönzők beépítésével kellene optimalizálnia.
Megfontolandónak tartják különböző ellenőrző pontok bevezetését is, amely segítséget nyújthat a kezelőorvosnak a betegút-menedzsment során.
Egyenlő hozzáférés
A beteg szociodemográfiai jellemzőitől független, egyenlő hozzáférés nem valósul meg tökéletesen. Az urológiai ellátás az országban centralizált, egy-egy nagy centrumra és számos kisebb szakrendelőre oszlik. A centrumokba való eljutáshoz nagyobb távolságot kell áthidalniuk a távolabb élő betegeknek, sok esetben ellátásukra nem is ezekben az intézményekben, hanem a közelebbi, kevésbé felszerelt szakrendelőkben kerül sor, így a területi egyenlőség kritériuma nem tud teljes mértékben teljesülni.
Betegközpontúság
A betegközpontúsággal kapcsolatban az interjúalanyok elmondták, hogy annak minősége elsősorban a szakemberek leterheltségén múlik. A hazai egészségügyben általánosan az orvosoknak, s így a prosztatarák ellátásában részt vevő szakembereknek is igen nagy a leterheltsége, így a szükségesnél kevesebb idő jut arra, hogy a beteg igényeit megismerjék, részletesen tájékoztassák és bevonják a kezelés, gyógyítás folyamatába.
Széles körű hozzáférés az innovációhoz
A nagyfokú életminőség-romlás elkerülése és a beteg állapotának szinten tartása az innovatív terápiák alkalmazásával biztosítható, amelyek egyre kedvezőbb életkilátásokat kínálnak a prosztatarákos betegeknek. Azoknak a betegeknek kisebb esélyük van a legmodernebb eljárások igénybevételére, akiket a kezelőorvosuk nem irányít át az innovatív terápiákat alkalmazó centrumokba.
Rehabilitáció
Jelenleg kevés figyelem irányul a betegek rehabilitációjára, aminek fő oka az egyéb társszakmák (gyógytornászok, pszichológusok és dietetikusok) limitált részvétele az ellátásban. Mivel a legtöbb urológiai centrumban ezen szakemberek megléte nem minimumfeltétel, így a prosztatarákos betegek ellátásában részvételük limitált.
Szintén korlátot jelent a palliatív személyzet elérhetősége: a rehabilitáció kulcsa lehet ezen szakemberek (palliatív nővér, szociális munkás, palliatív team) segítsége az ellátásban.
Onkoteam
Magasabb ellátási szinteken az onkoteamek hatékony működését azonosítottuk a legkritikusabb tényezőnek.
Az onkoteamekben a hatályos szabályozás szerint több szakmának kell képviseltetnie magát, ami a jelenlegi leterheltség mellett sok esetben komoly szervezési kérdéseket vet fel, főleg ott, ahol egyébként is kevés szakember áll rendelkezésre. Problematikus a beteg jelenléte is, ami a legtöbb esetben nem valósul meg.
Mindezek alapján fontos beavatkozási pont az onkoteamek hatékony működésének elősegítése.
Az onkoteamek a Covid-19-járvány alatt online formában működtek, ami a szakértői visszajelzések alapján sok esetben jelentősen megkönnyítette a szakemberek dolgát és praktikus volt azok számára, akik több intézmény onkoteamjében is részt vettek.
Optimalizálni kell a multidiszciplinaritást szolgáló onkoteamek működését, amelynek része az urológus, a patológus, a radiológus, a sugárterápiás szakorvos, az onkológus, a gyógytornász és ideális esetben a dietetikus és a pszichológus. Ahol ezen szakemberek megléte és jelenléte nem garantált, ott minden lehetséges eszközzel el kell érni, hogy az onkoteam ebben a legteljesebb körben összeülhessen. Az összeülés megkönnyítése céljából rendszeresíteni kell a világjárvány alatt bevetté vált online működést és fel kell tárni azokat a problémákat, amelyek akadályozhatják az onkoteamek működését.
Mindezek alapján megfontolandónak tartjuk az online onkoteamek gyakorlatának kiterjesztését, vagy másik megoldásként az onkoteamek országos szintű centralizálását. A centralizáció keretében az onkoteamek akár regionálisan is szerveződhetnének, kiküszöbölve a szakemberhiányt.
A betegek túlélésének meghosszabbítása és az életminőségük javulása érdekében kiemelten fontos, hogy összhangban az előírásokkal, az onkoteamek minden beteg esetében összehívásra kerüljenek (20).
A hazai prosztatarák-ellátás összefoglaló értékelése
Ahogy azt a fentebb bemutatott fejezetek is szemléltetik, a prosztatarák ellátása igen összetett, a problémák feloldása túltesz a jelen dokumentum keretein.
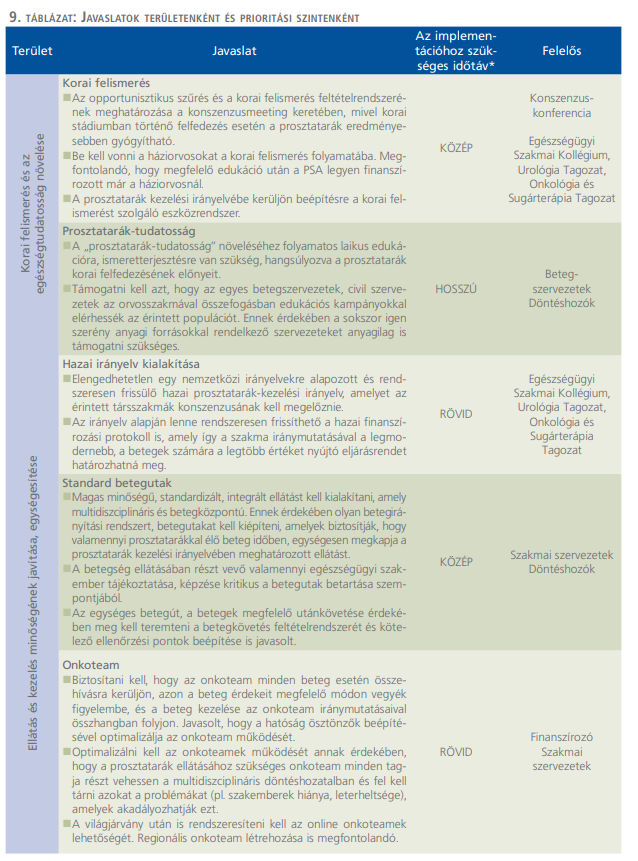
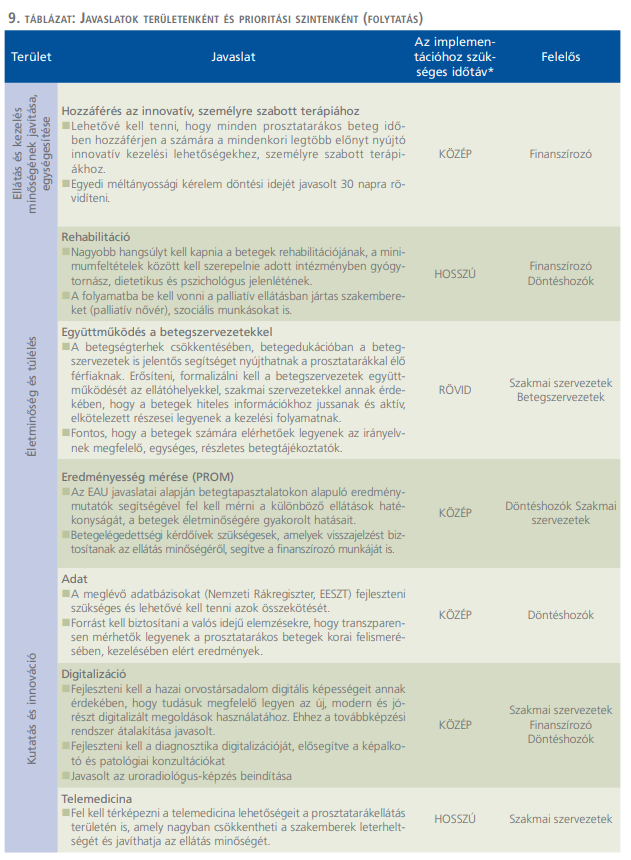
A valamennyi beteg számára elérhető, magas minőségű, standardizált, multidiszciplináris, betegközpontú ellátás kialakításához a következő prioritások átgondolása javasolt a társszakmák, döntéshozók, finanszírozó által (9. táblázat).
Köszönetnyilvánítás
Köszönettel tartozunk a kutatást segítő szakorvosoknak, egészségügyi szakembereknek (szakdolgozó, pszichológus, gyógytornász, háziorvos), valamint a felkeresett betegszervezetek képviselőinek, akik a tanulmány helyzetértékelési fázisában segítették munkánkat:
Dr. Ágoston Péter (Országos Onkológiai Intézet, Sugárterápiás Osztály, Budapest); Prof. Dr. Bajory Zoltán (Szegedi Tudományegyetem, Szent-Györgyi Albert Klinikai Központ, Urológiai Klinika); Dr. Beöthe Tamás (Péterfy Kórház-Rendelőintézet Országos Traumatológiai Intézet, Urológiai Osztály, Budapest); Dr. Biró Krisztina (Országos Onkológiai Intézet, Gyógyszerterápiás Központ, Budapest); Bognár Krisztina (Semmelweis Egyetem, Urológiai Klinika, Budapest); Dr. Désfalvi Judit (Semmelweis Egyetem, I. Sz. Belgyógyászati és Onkológiai Klinika, Budapest); Prof. Dr. Engert Zoltán Vendel (Markusovszky Egyetemi Oktatókórház, Urológiai-sebészeti Osztály, Szombathely); Dr. Kalina Ildikó (Semmelweis Egyetem, Orvosi Képalkotó Klinika, MR Diagnosztikai Részleg, Budapest); Kalotay Gábor (Gyógyulj Velünk Egyesület); Kapitány Zsuzsanna (Semmelweis Egyetem, Egészségtudományi Kar, Budapest); Dr. Nagy János (Zsolt utcai háziorvosi rendelő – I. kerület, Budapest); Dr. Pikó Béla (Békés Megyei Központi Kórház, Megyei Onkológiai Centrum, Gyula); Rozványi Balázs (Magyar Rákellenes Liga); Dr. Szarvas Tibor (Semmelweis Egyetem, Urológiai Klinika, Budapest); Dr. Tóth Erika (Országos Onkológiai Intézet, Daganatpatológiai Központ, Budapest)
Irodalom
1. Nyirády P. A prosztatarák sebészi kezelése. Magyar Onkológia 2019; 63: 26−31.
2. European Association of Urology (2020). White Paper on Prostate Cancer- Recommendations for the EU Cancer Plan to tackle Prostate Cancer.
3. Szendrői M. A prosztatadaganat. Magyar Orvos 2012; 8–9: 18−21.
4. Maráz A, Géczi L, Bíró K, et al. Terápiás szekvenciák az előrehaladott/ áttétes prosztatadaganatok gyógyszeres kezelésében. Magyar Onkológia 2020; 64: 263–272.
5. Globocan, 2018−2020.
6. Nemzeti Rákregiszter
7. Institute for Health Metrics and Evaluation Global Health Data Exchange, 2020.
8. KSH, 2020.
9. Eurostat Database, 2020 https://ec.europa.eu/eurostat/databrowser/ view/HLTH_CD_ASDR2_custom_167546/bookmark/table?lang=en&boo kmarkId=fd1d9607-b57f-4f6b-b081-86bc004aa1d8
10. Rencz F, Brodszky V, Varga P, et al. A prosztatarák gazdasági terhe nagy betegregiszterek alapján – Irodalmi áttekintés. Orvosi Hetilap 2014; 155(13): 509−520. https://doi.org/10.1556/OH.2014.29837
11. Luengo-Fernandez R, Leal J, Gray A. Economic burden of cancer across the European Union: a population-based cost analysis. Lancet Oncology 2013; 14(12): 1165−1174.
12. Healthware, 2014. https://doi.org/10.1016/S1470-2045(13)70442-X
13. 2019-es Zárszámadási törvény
14. Gulácsi L. Egészség-gazdaságtan és technológiaelemzés. Medicina; 2012.
15. Kósa Z. Egészségpolitika. Debreceni Egyetem Egészségügyi Kar; 2014.
16. Jayadevappa R, Schwartz JS, Chhatre S, et al. The Burden of Out-of-Pocket and Indirect Costs of Prostate Cancer. The Prostate 2010; 70: 1255–1264. 1. https://doi.org/10.1002/pros.21161
17. OEP. A prosztatarák diagnosztikájának és kezelésének finanszírozási protokollja. 2011.
18. Nelson W, Antonarakis E, Carter H, et al. Abeloff’s Clinical Oncology (Sixth Edition) − Prostate Cancer. Elsevier; 2020. https://doi.org/10.1016/B978-0-323-47674-4.00081-5
19. NEAK, gyógyító-megelőző ellátás
20. Géczi L. A prosztatarák diagnózisa és gyógyszeres kezelése. Interdiszciplináris Magyar Egészségügy 2014; 13: 5−8.
21. Wanner M, Richard A, Matthes K, et al. Trends in prostate cancer incidence between 1996 and 2013 in two Swiss regions by age, grade, and T-stage. Cancer Causes & Control 29:269–277, 2018. https://doi.org/10.1007/s10552-017-0993-9
22. Li J, Siegel DA, King JB. Stage-specific incidence rates and trends of prostate cancer by age, race, and ethnicity, United States, 2004-2014. Annals of epidemiology 2018; 28(5): 328–330. https://doi.org/10.1016/j.annepidem.2018.03.001
23. Patasius A, Smailyte G. Changing Incidence and Stage Distribution of Prostate Cancer in a Lithuanian Population-Evidence from National PSA-Based Screening Program. International journal of environmental research and public health 2019; 16(23): 4856. https://doi.org/10.3390/ijerph16234856
24. KSH. Tehetünk az egészségünkért, 2020.
25. Bíró K. A prosztatarák epidemiológiája. Interdiszciplináris Magyar Egészségügy 2013; 12(3): 48−54.
26. 31/2010. (V. 13.) EüM rendelet a finanszírozási eljárásrendről
27. Bíró K, Kun E, Dobi E. Élet prosztatarákkal a betegek szemszögéből. Egy hazai felmérés eredménye. Magyar Urológia 2019; 31(3): 91−97.
28. Bíró K, Géczi L. A mozgás szerepe a prosztatarák megelőzésében és kezelésében. Magyar Onkológia 2019; 63: 60–64.
29. Wilt TJ, Vo TN, Langsetmo L, et al. Radical Prostatectomy or Observation for Clinically Localized Prostate Cancer: Extended Follow-uo of the Prostate Cancer Intervention Versus Observation Trial (PIVOT). European Urology 2020; 77(6): 713−724. https://doi.org/10.1016/j.eururo.2020.02.009
30. Mottet N, Cornford P, van den Bergh RCN, et al. EAU-EANM-ESTRO- ESUR-ISUP-SIOG GUIDELINES ON PROSTATE CANCER. European Association of Urology 2021.