Complex therapy of spondylodiscitis developed on the basis of xanthogranulomatous pyelonephritis
DOI: 10.22591/magyurol.2021.2.antalt.75
Authors:
Antal Tamás dr., Osváth Péter dr., Szűcs Miklós dr.
Debreceni Egyetem, Klinikai Központ, Kenézy Gyula Campus, Urológiai és Andrológiai Osztály, Debrecen (osztályvezető: Szűcs Miklós dr.)
Summary
Introduction: Xanthogranulomatous pyelonephritis is a rare kind of chronic pyelonephritis, which usually caused by chronic urinary obstruction. According to literatures, xanthogranulomatous pyelonephritis is uncommon with a low percentage of the haematogenic spread, and no announcement of spondylodiscitis with such background has been found. The aim of this paper is to present the complex therapy of thoracic spondylodiscitis based on xanthogranulomatous pyelonephritis developed on the basis of impacted ureteral stone.
Case report: A 78-year-old male with paraplegia and uroszepszis was transferred to Emergency Department of Kenezy County Hospital for examination. Abdominal ultrasound showed left ureteral stone with diffuse dilation of the ureter and the renal pelvis. Lab tests resulted in higher inflammatory markers, impaired renal function and massive pyuria in the urine. Percutaneous nephrostomy was performed through an urgent operation immediately after a failed double-J insertion. After neurological and neurosurgical consultation, an urgent vertebral MRI was performed, consequently spondylodiscitis was found on the level of Th. X-XI Vertebrae; this was later proved by a CT guided core biopsy. Due to repeated neurosurgical and infectological consultation, primer decompressive operation was not available. Hence, the patient was given broad-spectrum antibiotics for six weeks. Control MRI showed mild regression of the thoracal spondylodiscitis. After a dynamic renal scan, nephrectomy via dorsal lumbotomy incision was performed and the histology proved the Xanthogranulomatous pyelonephritis was present. The rehabilitation started during the hospital stay and continued after hospital discharge by physiotherapists. During follow ups regression of neurological symptoms were found. Although the lower limb paraplegia is partly solved, the patient remained bed-bound.
Conclusion: This case report indicates that even in a typical occlusion case with severe neurological symptoms, neurological and neurosurgical consultations are necessary soon after an urgent urinary deviation. If spondylodiscitis is diagnosed 24-36 hours after the presentation of neurological symptoms, a decompressive operation is feasible. However, after this period, even with the neurosurgical procedure, full recovery cannot be achieved. Nonetheless, once spondylodiscitis is diagnosed, interdisciplinary approach is mandatory in order to eliminate the source of infection, avoid potential irreversible neurological complications and as a result, improving the patient’s quality of life.
LAPSZÁM: MAGYAR UROLÓGIA | 2021 | 33. ÉVFOLYAM, 2. SZÁM
Összefoglalás
Bevezetés: A xantogranulomatosus pyelonephritis egy ritkán előforduló krónikus pyelonephritis-variáns, amelynek hátterében leggyakrabban krónikus vizeletelfolyási obstrukció áll. Az irodalmi adatokat áttekintve a xantogranulomatosus pyelonephritis haematogen szóródása az esetek kis százalékában fordul elő és ily módon kialakult spondylodiscitisről közleményt nem találtunk. Dolgozatunkban egy impaktálódott uréterkő talaján kialakult xantogranulomatosus pyelonephritis és szövődményként jelentkező thoracalis spondylodiscitis komplex ellátását ismertetjük.
Esetismertetés: A 78 éves férfi beteg kivizsgálása paraplegia, illetve uroszepszis miatt kezdődött. Hasi UH-n a bal oldali uréterben kő ábrázolódott diffúz vese- és urétertágulat mellett. Laborvizsgálatban jelentősen emelkedett gyulladásos és vesefunkciós értékek igazolódtak, vizeletüledékben masszív pyuria került leírásra. Sürgősséggel bal oldali perkután nephrostoma-behelyezést végeztünk sikertelen DJ-katéter-fixálást követően. Paraplegia miatti kivizsgálás során neurológussal és idegsebésszel is konzultáltunk, sürgős gerinc-MRI-felvételen Th. X-XI. csigolyák magasságában spondylodiscitis igazolódott, amelyet CT-vezérelt biopszia is megerősített. Tekintettel a több napja fennálló paraplegiára primer dekompressziós műtét nem jött szóba, így infektológus javaslatára 6 hetes széles spektrumú antibiotikumterápiát indítottunk, amely után kontroll-MRI a thoracalis spondylodiscitis mérsékelt regresszióját mutatta. Dinamikus veseszcintigráfia alapján később lumbotomiás behatolásból nephrectomiát végeztünk, a szövettan xantogranulomatosus pyelonephritist igazolt. Kontrollvizsgálatok alkalmával betegünk állapota jelentősen javult, bár továbbra is ágyban fekvő, alsóvégtagi paraplegiája részben oldódott, rehabilitációja megkezdődött.
Következtetés: Esetbemutatásunk felhívja a figyelmet arra, hogy az urológiai gyakorlatban mindennaposnak számító veseokklúzió mellett jelentkező neurológiai tünetek esetén a sürgős vizeletdeviációt követően mihamarabbi neurológiai és idegsebészeti kivizsgálás szükséges. Amennyiben spondylodiscitis igazolódik, a neurológiai tünetek jelentkezésétől számítva 24-36 órán belül dekompressziós műtét végezhető, ezen időablakot átlépve azonban az idegsebészeti műtéttől a tünetek megszűnése már nem várható. A diagnózis felállítását követően több társszakma együttes bevonásával történik a kezelés, amelynek célja a potenciálisan irreverzibilis neurológiai szövődmények elkerülése, az infekció forrásának megszüntetése, illetve a beteg életminőségének javítása.
Bevezetés
A xantogranulomatosus pyelonephritis egy ritkán előforduló krónikus pyelonephritis-variáns, amelynek hátterében leggyakrabban krónikus vizeletelfolyási obstrukció áll. Az irodalmi adatokat áttekintve a xantogranulomatosus pyelonephritis haematogen szóródása az esetek kis százalékában fordul elő és ily módon kialakult spondylodiscitisről közleményt nem találtunk. Dolgozatunkban egy impaktálódott uréterkő talaján kialakult xantogranulomatosus pyelonephritis és szövődményként jelentkező thoracalis spondylodiscitis komplex ellátását ismertetjük.
Esetismertetés
A 78 éves férfi beteg anamnéziséből diabetes mellitus, hipertónia és nyílt cholecystectomia emelhető ki. 2020 nyarán kezdődött kivizsgálása egy hete fennálló bal oldali deréktáji fájdalom, négy napja meglévő, döntően jobb oldali paraplegia és uroszepszis miatt.
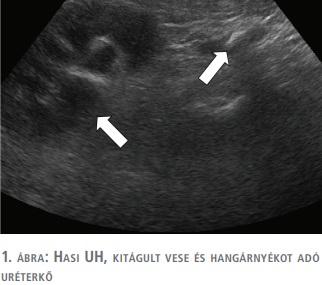
Kivizsgálása során laborvizsgálatban jelentősen emelkedett CRP, beszűkült vesefunkciós értékek, vizeletüledékben masszív pyuria igazolódott. Hasi ultrahangon (UH) (1. ábra) a bal uréter felső szakaszán egy 1 cm-es kő ábrázolódott, ettől proximálisan az uréter és az üregrendszer is diffúz tágulatot mutatott.
Felvételét követően sürgős bal oldali vizeletdeviációt végeztünk. Ennek során DJ-katétert kíséreltünk meg fixálni, azonban a korábban leírt uréterkő mellett drótot nem sikerült felvezetni, retrográd töltés során teljes stop ábrázolódott, így perkután nephrostoma (PNS) behelyezésével komplettáltuk a műtétet. Nephrostomán keresztül purulens váladék ürült, amelynek tenyésztési eredménye alapján (Staphylococcus aureus) ex juvantibus széles spektrumú, majd célzott antibiotikumterápiát indítottunk.
Zavartalan posztoperatív szakot követően a PNS néhány napig vezetett, majd elapadt, ezért anterográd töltést végeztünk, amely során a behelyezett pigtail jó helyzetben ábrázolódott. UH során a korábbi vesetágulat megszűnt. Kontroll-laborvizsgálatban mind a CRP, mind a vesefunkciós értékek jelentősen javultak.
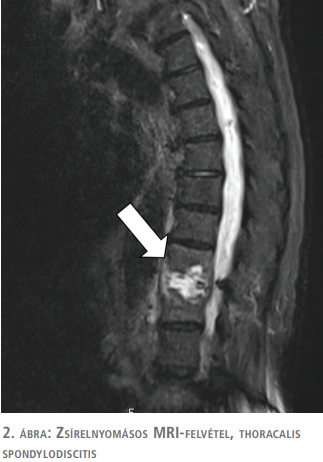
További terápiás terv felállítása céljából kontrasztos hasi és kismedencei CT-vizsgálat készült, amelyen jó helyzetben lévő PNS-t, elfolyási akadályt okozó uréterkövet, valamint bal oldali pyonephrost véleményeztek kontrasztanyag kiválasztása nélkül. Tekintettel a már felvételét megelőzően kialakult paraplegiára, neurológussal és idegsebésszel konzultálva sürgős gerinc-MRI (2. ábra) készült, amelyen Th. X-XI. csigolyák magasságában spondylodiscitisre jellemző morfológiai eltérést véleményeztek paravertebralis lágyrész-érintettséggel tályog jelenléte nélkül. Idegsebészeti konzílium szerint a több mint egy hete fennálló paraplegia miatt primer dekompresszió már nem jön szóba, így a spondylodiscitis célzott konzervatív kezelését javasolta CT-vezérelt biopsziát követően. CT-vezérelt mintavétel során aspirációs citológia nem volt kivitelezhető, azonban a core biopszia szövettana a spondylodiscitist megerősítette, így infektológiai javaslatra hat hétig tartó intravénás cefazolinterápiát indítottunk.
A thoracalis gerincszakaszt érintő folyamat primer forrása feltételezhetően a bal oldali pyonephros lehetett haematogen szóródás útján, azonban további góc kizárása céljából transthoracalis és transoesophagealis szív-UH is készült, amelyek eredménye mindkét esetben negatív lett. Dinamikus veseszcintigráfia során számottevő funkciót nem mutató bal oldali vese igazolódott (bal-jobb aktivitás 15-85%), így megfelelő előkészítést követően a felvételt követő hatodik héten lumbotomiás behatolásból nyílt veseeltávolítást végeztünk.
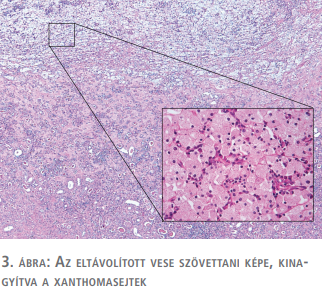
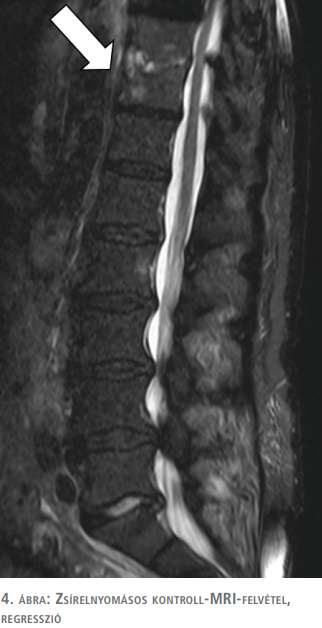
Az eltávolított vese patológiai vizsgálata során xantogranulomatosus pyelonephritis (3. ábra), egy igen ritka krónikus pyelonephritis-variáns igazolódott. Az antibiotikumterápia végeztével kontroll-MRI készült, amelyen a spondylodiscitis mérsékelt regresszióját véleményezték (4. ábra). A spondylodiscitis diagnózisának felállítása után a meglévő alsóvégtagi bénulás miatt komplex rehabilitáció kezdődött gyógytornászok bevonásával, ami hazabocsátást követően is folytatódott. Kontrollvizsgálatok alkalmával betegünk a deréktáji panaszok megszűnéséről számolt be, lumbotomiás sebe per primam gyógyult, paraplegiája részben oldódott, azonban továbbra is ágyban fekvő.
Megbeszélés
A xantogranulomatosus pyelonephritis (XGP) egy ritkán előforduló, a veseparenchyma krónikus destruktív granulomatosus gyulladását okozó folyamat, amelyet először Schlagenhaufer írt le 1916-ban (1). Patomechanizmusának hátterében legtöbbször krónikus obstrukció talaján létrejött infekció áll. Az esetek döntő többségében a vizeletelfolyási akadály oka a pyelont kitöltő korallkő, de kiváltó tényezőként PU-határ-szűkület, uréterkő vagy -tumor, hólyagtumor, illetve krónikus interstitialis nephritis is szerepelhet. A betegség általában középkorú nőket érint (férfi:nő arány 1:2), ugyanakkor az életkori előfordulása széles spektrumon mozog. Prediszponáló tényezők közül a diabetes mellitus, terhesség, hipertónia, rheumatoid arthritis, májcirrózis és az obesitas emelhető ki (1, 2).
Az XGP diagnózisának felállítása általában igen nehéz, tekintettel arra, hogy gyakran összetéveszthető egyéb krónikus pyelonephritisszel, vesetuberkulózissal, perinephricus tályoggal, sőt vesesejtes rákkal is (3, 4). Korkes és munkatársai által elvégzett, 41 esetet számláló tanulmányban mindössze 22%-ban (9 eset) volt gyanítható preoperatíve az XGP fennállása (4).
Legjellemzőbb tünetei a deréktáji fájdalom, illetve láz, továbbá fogyás, étvágytalanság, tapintható vesetáji terime és haematuria is gyakran megfigyelhető. Laborvizsgálatban legtöbbször leukocytosis, anémia, emelkedett CRP és beszűkült vesefunkció látható. Dwivedi és társai 2006-ban 21 esetet dolgoztak fel, amelynek során azt találták, hogy 95%-ban pyuria, 60%-ban pozitív vizelettenyésztés is előfordul a kivizsgálás során (5). A tenyésztési eredményekben leggyakrabban E. coli és Proteus mirabilis igazolódik, de leírták már Pseudomonas, Klebsiella, Enterococcus, illetve Candidatörzsek jelenlétét is.
Képalkotó vizsgálatok közül a legkönnyebben elérhető, a beteg számára sugárterhelést nem jelentő vizsgáló eljárás a hasi áttekintő ultrahang. Az érintett vese UH-vizsgálata során hydronephrosis, a normál veseparenchyma elvékonyodása, illetve sok esetben az okklúziót okozó, hangárnyékot adó kő látható. A diagnózis további pontosítása céljából hasi és kismedencei CT-vizsgálat elvégzése javasolt, amelynek során számos esetben láthatjuk az XGP-re jellemző, „medvetalphoz” („bear paw” sign) hasonlító kitágult vesekelyheket, továbbá tályog, kő jelenléte, valamint a vesén kívüli terjedés is jól azonosítható (3, 4, 6).
Bár a képalkotó eljárások a kivizsgálás során jelentős szereppel bírnak, azonban segítségükkel a diagnózis 100%-os biztonsággal nem állítható fel. Definitív diagnózis csakis a vesebiopszia vagy nephrectomia során nyerhető szövettani lelet birtokában lehetséges. A hisztológiai képre jellemzőek a lipidtartalmú histiocyták (xanthomasejtek), amelyek a veseparenchyma teljes egészét elfoglalhatják (1, 3, 5).
A XGP kezelése során döntő fontosságú a folyamat kiterjedtségének megítélése. A veseparenchyma érintettsége szempontjából diffúz és fokális formát különíthetünk el. Mintegy 80-85%-ban diffúz forma jelentkezik, ilyenkor nephrectomia elvégzése szükséges. A fokális XGP konzervatív kezeléssel (antibiotikumterápia), meghatározott esetekben perkután nephrostoma behelyezésével gyógyítható (2, 3). A krónikus gyulladás talaján a betegek mintegy egyharmadában szövődmények alakulnak ki, amelyek közül a legjelentősebbek a psoas és perinephricus abscessus, a nephro-cutan és nephro-colicus fistula, valamint a szepszis (2, 3).
Az irodalmi adatokat áttekintve eddig még nem közöltek XGP-vel egyidejűleg jelentkező, feltételezhetően haematogen szóródás útján kialakult spondylodiscitist. Ismertek viszont egyéb patogenezisű és kórlefolyású, a vesét érintő gyulladásos kórképek, amelyek esetünkhöz hasonlóan az Adamkiewicz-artérián keresztül érik el és fertőzik meg a thoracalis IX-XII-es gerincszakaszt. A spondylodiscitis egy ritkán előforduló infektív megbetegedés, amely az intervertebralis discust és a szomszédos csigolyatesteket érinti (7). Hajlamosító tényezők közül a diabetes mellitus, immunszuppresszív állapotok, intravénás droghasználat, HIV-fertőzés és az időskor emelhető ki (8).
Kialakulásának hátterében haematogen disszemináció, külső ráterjedés, illetve a környező szövetekből történő direkt terjedés játszhat szerepet. Legtöbbször a haematogen forma fordul elő, primer gócként általában a húgyúti traktus infekciói, szívbillentyűn kialakult vegetáció, infektálódott nagyvéna-katéter, diverticulitis, illetve cellulitis szerepelnek (9).
A tünetek közül domináló a háti fájdalom, amely az esetek több mint 90%-ában jelen van és általában a lumbalis szakaszt érinti, továbbá 48-63%-ban jelen van láz is (9, 10). Neurológiai szövődmények, mint gyöki és gerincvelő-kompresszió az esetek 1/3-ában jelentkezik; ellátásuk a tünetek kezdetétől számítva 24-36 órán belül szükséges, ellenkező esetben a folyamat irreverzibilissé válik (10). Laborvizsgálatban jellemző a mérsékelt CRP- és leukocitaszám-emelkedés, valamint a gyorsult vörösvértest-süllyedés. Spondylodiscitis gyanúja esetén legalább két pár hemokultúra levétele szükséges. Empirikus kezelést követően a patogének detektálása 25-59%-os valószínűséggel lehetséges, ellenkező esetben ez a szám akár a 70%-ot is meghaladhatja (8).
Azon betegeknél, akik hemodinamikailag stabilak, nem észlelhető szepszis, szeptikus sokk és nincsenek progresszív neurológiai tünetek, az antibiotikumterápia elindítása késleltethető a mikrobiológiai mintavétel eredményéig (8, 10). Európában a leggyakrabban előforduló kórokozó a Staphylococcus aureus, amely az esetek több mint 50%-ában fordul elő, ezt követik a Gram-negatív patogének mint például az Escherichia coli, világviszonylatban pedig a Mycobacterium tuberculosis vezető szerepe figyelhető meg (8).
A spondylodiscitis diagnózisának felállítása szempontjából döntő fontosságú az MRI-vizsgálat elvégzése, amelyet minden neurológiai tünettel rendelkező beteg esetén ajánlott elvégezni (7, 8, 9, 10). Egy 103 beteget vizsgáló tanulmányban leírták, hogy a tünetek jelentkezésétől számítva két héten belül az MRI szenzitivitása 91%, több hetes panaszok esetén ugyanez már 96% is lehet (9). A spondylodisictis diagnózisa során a CT-vizsgálat kevésbé érzékeny, azonban a szövettani vizsgálathoz szükséges mintavétel általában CT-vezérelten történik, ilyenkor core-biopszia és aspirációs citológia is kivitelezhető. A mikrobiológiai mintavétel eredményét követően célzott hat hétig tartó széles spektrumú kezelés kezdődik, legtöbbször béta-laktám antibiotikumokkal (7, 8).
A komplex kezelés célja minden esetben a fertőzés forrásának eliminálása, a neurológiai károsodások helyreállítása, illetve a fájdalom csökkentése. Hetente legalább egy alkalommal szükséges laborkontroll, illetve neurológiai vizsgálat a tünetek alakulása, illetve a kezelésre adott válasz megítélése céljából. Abban az esetben, ha négy hét elteltével a tünetek rosszabbodnak vagy változatlanok maradnak, akkor ismételt gerinc-MRI elvégzése szükséges a folyamat kiterjedtségének feltérképezése, illetve a szövődmények jelentkezésének mihamarabbi felderítése céljából (8).
Következtetések
Esetbemutatásunk felhívja a figyelmet arra, hogy az urológiai gyakorlatban mindennaposnak számító veseokklúzió mellett jelentkező neurológiai tünetek esetén a sürgős vizeletdeviációt követően mihamarabbi neurológiai és idegsebészeti kivizsgálás szükséges. Amennyiben spondylodiscitis igazolódik, a neurológiai tünetek jelentkezésétől számítva 24-36 órán belül dekompressziós műtét végezhető, ezen időablakot átlépve azonban az idegsebészeti műtéttől a tünetek megszűnése már nem várható (10). A diagnózis felállítását követően több társszakma együttes bevonásával történik a kezelés, ennek során legalább hat hétig tartó széles spektrumú antibiotikumkúra elindítása, illetve a primer góc, jelen esetünkben a tályogos bal oldali vese eltávolítása szükséges a potenciálisan irreverzibilis neurológiai szövődmények elkerülése, illetve a beteg életminőségének javítása céljából.
Az elkövetkező évtizedekben az általunk ismertetett kórállapotok előfordulása várhatóan növekedni fog, tekintettel a magyar társadalmat is érintő elöregedésre, az invazív beavatkozások, illetve immunszuppresszív kezelések számának növekedése miatt.
References
1. Li L, Parwani AV. Xanthogranulomatous pyelonephritis. Arch Pathol Lab Med 2011 May; 135(5): 671–4.
doi: 10.1043/2009-0769-RSR.1. PMID: 21526966
2. Çaliskan S, Özsoy E, Kaba S, Koca O, Öztürk MI. Xanthogranulomatous Pyelonephritis. Arch Iran Med 2016 Oct; 19(10): 712–714. PMID: 27743436
3. Jha SK, Aeddula NR. Pyelonephritis Xanthogranulomatous. [Updated 2020 Dec 1]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2020 Jan. Available from:
https://www.ncbi.nlm.nih.gov/books/NBK557399/
4. Korkes F, Favoretto RL, Bróglio M, Silva CA, Castro MG, Perez MD. Xanthogranulomatous pyelonephritis: clinical experience with 41 cases. Urology 2008 Feb; 71(2): 178–80.
doi: 10.1016/j.urology.2007.09.026. PMID: 18308077
5. Craig WD, Wagner BJ, Travis MD. Pyelonephritis: radiologic-pathologic review. Radiographics. 2008 Jan-Feb; 28(1): 255–77; quiz 327-8.
doi: 10.1148/rg.281075171. PMID: 18203942
6. Lee JH, Kim SS, Kim DS. Xanthogranulomatous Pyelonephritis: “Bear’s Paw Sign”. J Belg Soc Radiol 2019 May 13; 103(1): 31.
doi: 10.5334/jbsr.1807. PMID: 31139769; PMCID: PMC6524550
7. Lestin-Bernstein F, Tietke M, Briedigkeit L, Heese O. Diagnostics and antibiotic therapy for spondylodiscitis, Journal of Medical Microbiology 2018; 67: 757–768.
doi: 10.1099/jmm.0.00070
8. Herren C, Jung N, Pishnamaz M, Breuninger M, Siewe J, Sobottke R. Spondylodiscitis: Diagnosis and Treatment Options. Dtsch Arztebl Int 2017 Dec 25; 114(51–52): 875–882.
doi: 10.3238/arztebl.2017.0875. PMID: 29321098; PMCID: PMC5769318
9. Amini MH, Salzman GA. Infectious spondylodiscitis: diagnosis and treatment. Mo Med 2013 Jan-Feb; 110(1): 80–4. Erratum in: Mo Med 2013 Mar-Apr; 110(2): 121. Erratum in: Mo Med 2013 Mar-Apr; 110(2): 121. PMID: 23457758; PMCID: PMC6179648
10. Gregori F, Grasso G, Iaiani G, Marotta N, Torregrossa F, Landi A. Treatment algorithm for spontaneous spinal infections: A review of the literature. J Craniovertebr Junction Spine 2019 Jan-Mar; 10(1): 3–9.
doi: 10.4103/jcvjs.JCVJS_115_18. PMID: 31000972; PMCID: PMC6469318