Challenges of curative treatment of prostate carcinoma during the Covid-19 pandemic
DOI: 10.22591/magyurol.2022.3.darabosn.102
Authors:
Darabos Norbert dr., Szepesváry Zsolt dr., Kullmann Tamás dr.
Petz Aladár Egyetemi Oktató Kórház, Osztályológiai, Győr (osztályvezető: Szepesváry Zsolt dr.)
Summary
Objective: The Covid-19 pandemic caused by Covid-19 in Hungary also significantly changed the algorithms used in the diagnosis and treatment of prostate cancer. It can be hypothesized that this change had a negative effect on patients’ chances of recovery.
Material and methods: Data from laparoscopic radical prostatectomies performed during the epidemic were compared with those performed during peacetime. Data from 19 patients operated on between October 2019 and January 2020 in normal healthcare were analyzed. The average time from diagnosis to surgery was 3 months.
As a control, data from 16 patients operated between October 2020 and January 2021 were processed. The average time from diagnosis to surgery was 4 months during epidemic. The prostate biopsy findings, the predictive risk of lymph node involvement calculated from the Briganti nomogram, final histological findings, and postoperative PSA values of the patients were recorded. If the patient received ADT prior to surgery for any reason, it was also recorded.
PSA values were monitored postoperatively for 6 months in both groups, and early biochemical relapse was examined. PSA laboratory tests were performed 3 and 6 months after surgery. The cut-off level was determined in 0.1 ng/ml.
Results: The data showed that during the Covid-19 pandemic, prostate tumour patients were diagnosed and treated with more severe stage of the disease meaning higher preoperative and postoperative Gleason score values, and a more advanced pathological stage. Local extent at the pT3 stage was 2.97-fold more common than those who were operated before the pandemic period.
Consequently, the rate of positive surgical margin was also higher in the pandemic group. Perineural spread was found to be 2.57-fold and lymhovascular invasion was 2.37-fold. There was also a significant difference in the rate of early biochemical relapse, which was also higher in the pandemic group.
Conclusion: The results indicate that patients have a lower chance of cancer-specific recovery during the Covid-19 pandemic. Due to the delay or omission of screening programs, patients may be diagnosed and treated later.
LAPSZÁM: MAGYAR UROLÓGIA | 2022 | 34. ÉVFOLYAM, 3. SZÁM
Összefoglalás
Célkitűzés: A Covid-19 okozta pandémia Magyarországon is jelentős mértékben megváltoztatta békeidőben, a prosztatarák kivizsgálása és kezelése során alkalmazott algoritmusokat. Azt feltételeztük, hogy ez a változás rontotta a betegek prosztatarák specifikus gyógyulási esélyét.
Anyag és módszer: Vizsgálatunkban a járvány alatt végzett laparoszkópos radikális prostatectomiák adatait hasonlítottuk össze a békeidőben végzett beavatkozásokéval.
2019. október és 2020. január között operált 19 beteg adatait elemeztük, akiknél az egészségügyi rendszer a szokott módon működött. A diagnózistól a műtétig eltelt idő átlagosan 3 hónap volt. Kontrollként 2020. október és 2021. január között operált 16 beteg adatait dolgoztuk fel. Ezen páciensek hozzáférése a járóbeteg-ellátáshoz csökkent, a diagnózistól a műtétig eltelt idő 4 hónap volt. A pácienseknél rögzítettük a biopszia eredményét, a Briganti-nomogram alapján számított kockázati értéket, a végleges szövettani lelet adatait és a posztoperatív PSA-értékeket. Ha a beteg kapott ADT-t a műtét előtt bármilyen okból, azt is feljegyeztük.
Posztoperatívan 6 hónapig követtük mindkét csoportban a PSA-értéket, a korai biokémiai relapszust vizsgáltuk. A műtétet követően 3 és 6 hónappal végeztünk PSA-laborvizsgálatot. A cut-off level-t 0,1 ng/ml-ben határoztuk meg.
Eredmények: Az eredmények alapján megállapítható volt, hogy a Covid-19-pandémia idején a prosztatatumoros betegek előrehaladottabb betegséggel, magasabb preoperatív és posztoperatív Gleason-score értékekkel és előrehaladottabb patológiai stádiummal kerültek műtéti ellátásra osztályunkon. A pT3-stádiumú lokális kiterjedtség 2,97-szor gyakoribb volt a járvány alatti időszakban operáltaknál. Ebből következően a pozitív sebészi szél aránya is magasabb volt a pandémiás csoportban. A perineurális terjedés 2,57-szor, a limfovaszkuláris invázió 2,37-szor fordult elő többször. Szignifikáns eltérést mutatott a korai biokémiai relapszus aránya is, amely szintén a járvány alatti csoportban volt a magasabb.
Megbeszélés: A fenti eredmények rámutatnak arra, hogy pandémia idején a betegek rákspecifikus gyógyulási esélye kisebb. A szűrővizsgálatok csúszása, illetve elmaradása miatt a páciensek eleve később kerülnek kuratív ellátásra.
Bevezetés
A Covid-19-járvány Magyarországon nagyobb megbetegedési számokkal először 2020. szeptemberben jelent meg. A 2020. márciustól érvényes korlátozások viszont a szűrővizsgálatok és az egészségügyi kezelések korlátozott hozzáférését eredményezték, ugyanakkor még nagy mennyiségű Covid-19-fertőzött nem volt jelen. Bár az onkológiai kezelések megtörténtek, mind műtéti beavatkozások és kuratív irradiációk elvégezhetők voltak, azonban a megszokott kivizsgálási algoritmusok megbomlása miatt feltehetően a daganatos megbetegedések egy része nem került időben felismerésre.
Ezt a feltételezést támasztja alá egy Hollandiában végzett tanulmány, amely szerint a Covid-19-járvány alatt a daganatos betegségek csak kisebb számban és előrehaladottabb stádiumban kerültek látótérbe (2). A tapasztalt jelenség mögött több okot feltételeztek. Először is azok a betegek, akiknek nem specifikus tünetekkel jelentkezett a daganatos megbetegedése, valószínűleg nem konzultáltak háziorvosukkal, egyrészt azért mert nem akarták rabolni a háziorvos idejét nem Covid-19 megbetegedésre jellemző tünetekkel, vagy attól féltek, hogy a rendszer energiaforrásaira nagyobb szükség van ennél fontosabb nem Covid-19-fertőzéshez kapcsolt betegségekben is. Visszatarthatta őket a megfertőződéstől való félelem is.
Másodszor a háziorvosi ellátás javarészt telemedicina formájában történt, így ha a betegnek nem daganatra specifikus, gyanús tünete volt, a kivizsgálással valószínűleg vártak. Harmadszor, a kórházak Covid-19 által megnövekedett terhelése miatt hosszabb időbe teltek az egyébként rutinkivizsgálási folyamatok. Végül pedig 2020. március 16-án országosan leállították az emlő-, colorectalis és méhnyakrákszűrő programokat, hogy kapacitásokat szabadítsanak fel az egészségügyi rendszerben (2).
Daganatos betegek Covid-19-fertőzése
Figyelembe véve a korábbi publikációk eredményeit, bizonyos, hogy a daganatos betegek, illetve azok, akiknek kórtörténetében szerepel daganatos megbetegedés, fokozott kockázatnak vannak kitéve a Covid-19-fertőzés szempontjából. Több tanulmány eredményeit összevetve a daganatok összes prevalenciája a Covid-19-fertőzött betegek között 2%-nak (95% CI: 2,0%–3,0%; I2 = 83,2%) bizonyult.
Tekintettel arra, hogy az eredmények szerint tumor miatt 1 hónapon belül műtéten átesett vagy kemoterápiában részesülő betegek kockázata magasabb a súlyosabb kimenetelű Covid-19-fertőzésre (75% vs. 45%), 3 komoly kérdés merült fel
- Kellene-e arra törekednünk, hogy a stabil daganatos betegségben szenvedők elektív műtétjét vagy adjuváns kemoterápiáját halasszuk?
- Szorgalmaznunk kellene-e a daganatos betegek szigorúbb járványügyi védekezését?
- Nem kellene-e több szerepet adnunk az online tanácsadásra vagy kivizsgálásra és kezelésre a kritikus daganatos esetekben?
Liang és munkatársai (4) 1590 Covid-19-fertőzött kínai állampolgár adatainak feldolgozása során 1%-nak találta a daganat prevalenciát (95% CI: 0,61%–1,65%). Ez jóval magasabb a Kínai összpopuláció daganat prevalenciájánál (0,29%). Illetve, ami még fontosabb, a daganatos betegek kockázata jóval magasabb a súlyos klinikai kimenetelre (intenzív ellátás szükségessége és gépi lélegeztetés vagy halál) mint a daganatmenteseké (39% vs. 8%; hazard ratio (39% vs. 8%, HR=5,34; 95% CI: 1,80–16,18; p=0,0026). Egy másik, szintén Kínában végzett multicentrikus vizsgálat is alátámasztotta, hogy a daganatos betegek között magasabb a súlyos Covid-19-fertőzés aránya, és rosszabb a prognózis. A vizsgált betegségek közül a leggyakoribb daganattípus a tüdődaganat volt, és ez felelt legmagasabb arányban a Covid-19-fertőzéshez kapcsolható halálokért (33,3%, 5/15). A tanulmány alapján a prognózis jobb volt a követési szakaszban, mint az aktív onkológiai kezelés szakaszában (3).
ADT vs. Covid-19
A Covid-19-fertőzött populáció adatainak elemzése alapján feltűnő, hogy a férfiakban gyakoribb a súlyos kimenetelű fertőzés, ennek oka nem pontosan tisztázott. Azonban az androgén szenzitivitás modell magyarázatot adhat arra, miért alakulhat ki gyakrabban súlyos Covid-19-fertőzés a férfiakban, és miért vannak látszólag védve a gyermekek. Továbbá a rasszok közötti Covid-19-fertőzés mortalitás különbségére is magyarázatot ad. Az androgénreceptor szabályozza a transzmembrán proteáz-szerin 2 (TMPRSS2) transzkripcióját, ami szerepet játszik a SARS-CoV-2-infektivitásban. TMPRSS2 indítja meg a vírus tüskefehérjéjének traszkripcióját, aminek két következménye van: csökkenti a vírus felismerését az antitestek neutralizálásával, és aktiválja a SARS-CoV-2 vírus-sejt fúzióját (1. ábra) (7).
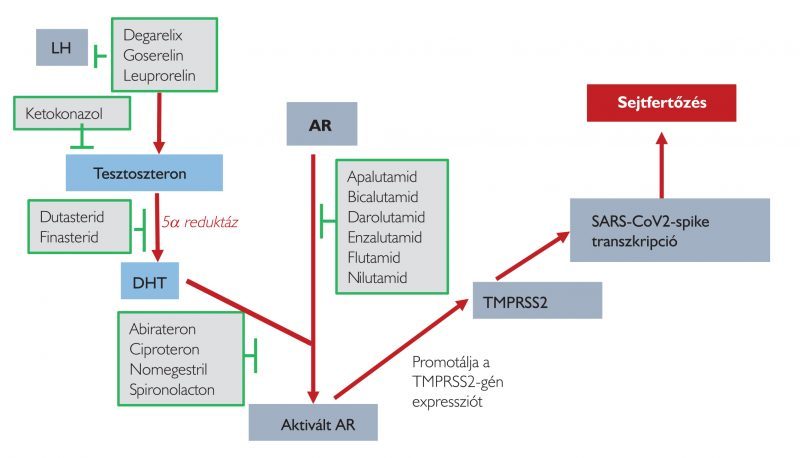
1. ábra: Androgén útvonal Covid-19-fertőzésben (7)
Ez alapján az olyan, magasabb androgénreceptor-aktivitással járó genetikai problémákból eredő betegségek, mint az androgén alopécia, prosztatarák, jóindulatú prosztatamegnagyobbodás és policisztásovárium-szindróma feltehetően magasabb fertőzésre való fogékonyságot okoznak. A teoretikus epidemiológiai és molekuláris mechanizmusok mellett, a közölt adatok alapján magas arányban fordul elő az androgén alopecia a súlyos tünetek miatt hospitalizált Covid-19-fertőzöttek között. Az androgénszenzitivitás feltehetően a meghatározója a Covid-19-fertőzés súlyosságának (7).
Mivel az androgén által szabályozott TMPRSS2-gén részt vesz a koronavírus sejtbe jutásában, azt feltételezték, hogy az ADT javíthatja a Covid-19-fertőzés kimenetelét.
Egy 2020-as multicentrikus tanulmányban több mint 120 onkológiai centrum prosztatarákkal és egyidejűleg Covid-19-fertőzéssel diagnosztizált 589 betegének adatait vizsgálták 2020. július 30-ig. Összességében magas volt a 30 napos halálozás (19%) és a súlyos Covid-19-fertőzés (28%) aránya a betegek között. Azonban nem találtak szignifikáns eltérést a Covid-19-fertőzés kimenetelében aszerint, hogy kap-e a páciens ADT-t vagy sem. A vizsgált gyógyszercsoportok közül a súlyos Covid-19-fertőzés (20%) és 30 napos halálozás (10%) az ARI-2-t (darolutamid, enzalutamid, apalutamid) kapó betegek között volt számszerűleg a legalacsonyabb, de kevés volt az esetszám (20 páciens) (5).
Mindemellett egy olaszországi tanulmány szignifikáns különbséget talált az ADT és Covid-19-fertőzés viszonylatában. 2020. április 1-jéig Veneto-ban 9280 SARS-CoV-2-pozitív beteget regisztráltak. Összességében a férfiak között több súlyos szövődmény fordult elő, gyakrabban kerültek kórházba és rosszabb klinikai kimenetük volt, mint a nőknek. Csak a veneto-i férfi lakosságot figyelembe véve (2,4 millió férfi), 0,2% és 0,3% volt a daganatmentes és daganatos betegek között a SARS-CoV-2-pozitivitás aránya. Összevetve az összes prosztatarákos beteg SARS-CoV-2-fertőzésének arányával, az ADT-ben részesülő betegek között szignifikánsan alacsonyabb volt a fertőzöttség, mint az ADT-ben nem részesülőknél (OR=4,05; 95% CI: 1,55–10,59). A másfajta daganatban szenvedők adatival összevetve pedig még magasabb volt a különbség az ADT-ben részesülők javára (OR=4,86; 95% CI: 1,88–12,56) (6).
Az eredmények azt sugallják, hogy annak ellenére, hogy a daganatos betegek fokozott fertőzéskockázatnak vannak kitéve, az ADT-ben részesülő betegek részben védve vannak a SARS-CoV-2-fertőzéssel szemben (5).
Betegek és módszer
2018. január és 2020. december között osztályunkon 138 laparoszkópos radikális prostatectomiát végeztünk. A betegek hozzáférése a szűrővizsgálatokhoz és a szakrendelésekhez 2020. februárig megfelelő volt, megegyezett az elmúlt évekkel. 2020. márciustól az egészségügyi rendszer a páciensek számára nehezen volt elérhető. A szűrővizsgálatok száma jelentősen csökkent, a járóbeteg-ellátás minimális szinten mozgott. Külföldön már jelentős számú Covid-19-megbetegedés volt, de Magyarországon a napi esetszámok a 100 főt sem lépték túl. A páciensek halogatták az orvoshoz fordulást.
Prosztatarák gyanúja esetén a magyar betegellátási rendszerben a szűrővizsgálatot követően átlagosan 2-4 héten belül történik meg a biopszia. Ezt követően a staging vizsgálatok újabb 2-4 hetet vesznek igénybe. Magyarországon kötelező az onkológus, urológus, radioterapeuta, patológus és radiológus részvételével megtartott ONKOTEAM döntése a kezelés megkezdéséhez. Ha radikális prostatectomia a döntés, a várakozási idő átlagosan 2-3 hónap.
A fentiek alapján az első vizsgálattól a kuratív műtéti kezelésig 2-5 hónap telik el. Ez az adat a pandémia előtti működésre vonatkozott.
Bár a Covid-19-járvány alatt a betegek száma csökkent, de az ellátórendszer kapacitása is kevesebb lett. A személyzet jelentős részét a Covid-19-ellátásra osztották be, a kevesebb betegre kevesebb orvos, diagnosztikus és műtéti lehetőség jutott.
A Covid-19-pandémia alatt a betegek hozzáférése az egészségügyi rendszerekhez rossz volt, emiatt késett a diagnózis és a megfelelő kezelés. Figyelembe véve a beteg megjelenésétől a kezelésig eltelt időt, megvizsgáltunk két időszakot a prosztatarákos betegek kezelésében.
2019. október és 2020. január között operált 19 beteg adatait elemeztük, akiknél az egészségügyi rendszer a szokott módon működött. A diagnózistól a műtétig eltelt idő átlagosan 3 hónap volt.
Kontrollként 2020. október és 2021. január között operált 16 beteg adatait dolgoztuk fel. Ezen páciensek hozzáférése a járóbeteg-ellátáshoz csökkent volt, a szűrővizsgálatok gyakorlatilag nem működtek. A műtéti kapacitás jelentősen csökkent, a fekvőbeteg-ellátásban a Covid-19 második hulláma miatt a dolgozók kis része tudott csak részt venni az onkológiai ellátásban. Elemzésünk alapján a diagnózistól a műtétig eltelt idő a pandémia alatt átlagosan 1 hónappal nyúlt meg, a diagnózistól a műtétig eltelt idő 4 hónap volt.
A pácienseknél rögzítettük a biopszia eredményét, a Briganti-nomogram alapján számított kockázati értéket, a végleges szövettani lelet adatait és a posztoperatív PSA-értékeket. Ha a beteg kapott ADT-kezelést a műtét előtt bármilyen okból, azt is feljegyeztük.
Posztoperatívan 6 hónapig követtük mindkét csoportban a PSA-értéket, korai biokémiai relapszust vizsgáltuk. A műtétet követően 3 és 6 hónappal végeztünk PSA-laborvizsgálatot. A cut-off level-t 0,1 ng/ml-ben határoztuk meg.
Magyarországon rutinszerűen sem a fúziós biopszia, sem a PSMA-PET CT nem elérhető a prosztatarák kivizsgáláskor, így a kockázatbecsléshez a 2012-ben megjelent Briganti-nomogramot használtuk. Ebben a nyirokcsomó-pozitivitás kockázat megítéléséhez szükséges adatok a következők: tapintási lelet (klinikai stádium), PSA-érték, Gleason-score, pozitív biopsziák száma. Ezeket az adatokat mind rögzítettük.
Minden esetben szaturációs biopsziát végeztünk 12 mintával. A prosztatabiopszia eredményéből a Gleason-score, a pozitív biopsziák aránya, illetve a karcinóma fajtája (pl. cribriform) került rögzítésre.
A műtétet követő szövettani vizsgálatból a patológiai stádiumot, a Gleason-score-t, a nyirokcsmó-eltávolítás esetén a pozitív nyirokcsomók számát, a perineurális és limfovaszkuláris inváziót, és a sebésziszél-pozitivitást vizsgáltuk. A 2020. október és december között operált minden betegnél a kórházi felvétel előtt Covid-19 PCR-tesztet végeztünk. Csak negatív eredmény esetén végeztük el a műtétet. Ebben az időszakban operált betegek közül egy sem esett át megelőzően a betegségen. A betegeket nemcsak onkológiai, hanem Covid-19 szempontból is követtük. Megvizsgáltuk, hogy átestek-e később a műtétet követően a Covid-19-megbetegedésen (2. ábra).
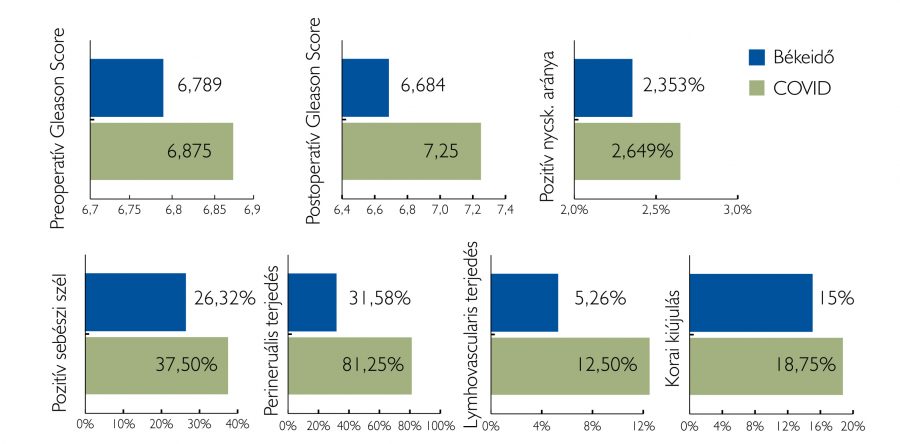
2. ábra: Covid előtt és Covid alatt radikális prostatectomián átesett betegek összehasonlító onkológiai adatai (Petz Aladár Kh. Győr)
Eredmények
A pandémia előtt 2019. október és 2020. január között 19 beteget operáltunk osztályunkon. A Briganti-nomogram alapján 6 esetben végeztünk kiterjesztett kismedencei lymphadenectomiát. Átlagosan 14,16 nyirokcsomót távolítottunk el, a pozitív nyirokcsomók aránya 2,353% volt. A preoperatív Gleason-score átlagban 6,789 volt, a posztoperatív 6,684-re adódott. A szövettani feldolgozást követően a patológiai stádiumok aránya százalékosan: pT1a: 5,26%; pT2a: 5,26%; pT2c: 84,21%; pT3b: 10,526%-nak bizonyult. Pozitív sebészi szél 5 esetben került kimutatásra (26,32%). Perineurális terjedés 31,58%-ban volt látható, míg limfovaszkuláris invázió 5,26%-ban. A korai biokémiai kiújulás aránya 15% volt 3 hónap után, amelynek aránya 6 hónapos utánkövetés során sem növekedett.
A pandémia alatt, 2020 októbere és 2021 januárja között 16 betegnél végeztünk radikális prostatectomiát és a Briganti-nomogram alapján 9 esetben végeztünk kiterjesztett kismedencei lymphadenectomiát. Az átlagosan eltávolított nyirokcsomók száma 16,77 volt, a pozitív nyirokcsomók aránya 2,649%-nak bizonyult. Az átlagos preoperatív Gleason-score 6,875, míg a posztoperatív 7,25 volt. A minták patológiai feldolgozása után a stádiumbesorolások a következőképpen alakultak: pT2a: 6,25%; pT2c: 50%; pT3a: 12,5%; pT3b: 31,25% (3. ábra). Pozitív sebészi szélt is magasabb arányban tapasztaltunk (37,5%). Perineurális terjedés rendkívül magas arányban (81,25%), míg limfovaszkuláris invázió 12,5%-ban jelent meg. A korai biokémiai kiújulás aránya 18,75%-nak bizonyult 3 hónap után, amely érték fél év után változatlan maradt.
A vizsgált betegcsoportokban a páciensek összesen 68%-a kapott a műtét előtt legalább egyszer LHRH-analóg injekciót. Viszont sem a pandémiás, sem a békeidőbeli csoportban nem fordult elő kórházi ellátást igénylő COVID-megfertőződés a vizsgált követési periódusban.
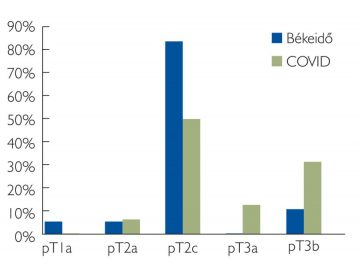
3. ábra: Patológiai stádiumok megoszlása
Megbeszélés
Az eredmények alapján megállapítható volt, hogy a Covid-19-pandémia idején a prosztatatumoros betegek előrehaladottabb betegséggel, magasabb preoperatív és posztoperatív Gleason-score értékekkel, és előrehaladottabb patológiai stádiummal kerültek műtéti ellátásra osztályunkon.
A pT3-stádiumú lokális kiterjedtség 2,97-szor gyakoribb volt a járvány alatti időszakban operáltaknál (3. ábra). Ebből következően a pozitív sebészi szél aránya is magasabb volt a pandémiás csoportban. A perineurális terjedés 2,57-szor, a limfovaszkuláris infiltráció 2,37-szor fordult elő többször.
Szignifikáns eltérést mutatott a korai biokémiai relapszus aránya is, amely szintén a járvány alatti csoportban volt a magasabb (2. ábra).
Mivel a vizsgált betegcsoportokban nem fordult elő ellátást igénylő Covid-19-megfertőződés sem az ADT-ben részesülő, sem a hormonterápia-naiv páciensekben, így nem tudtunk következtetést levonni az ADT Covid-19-megfertőződést befolyásoló hatásával kapcsolatban.
A fenti eredmények rámutatnak arra, hogy pandémia idején a betegek rákspecifikus gyógyulási esélye kisebb.
A szűrővizsgálatok csúszása, illetve elmaradása miatt a páciensek eleve később kerülnek kuratív ellátásra. A betegek szintén nem szívesen látogatnak a kórházakba, mert félnek a fertőzéstől.
A 2020-as EAU COVID-19-guideline ajánlása alapján a normál tapintatú, 10 ng/ml PSA-szint alatti betegeknél a biopszia, így a kivizsgálás is 6 hónappal halasztható. A guideline kiadását követően mindenki abban reménykedett, hogy a pandémia 6 hónapon belül véget ér és az egészségügyi rendszerek működése is helyreáll. Sajnos a pandémia elhúzódása miatt a halasztott ellátások elvégzése is szükségessé vált, a folyamatosan ismétlődő hullámok mellett az ellátások halasztásának ajánlását is folyamatosan újra kell értelmeznünk.
Irodalom
1. Desai ASS. COVID-19 and Cancer: Lessons From a Pooled Meta-Analysis. JCO GlobOncol 2020; 557–559. https://doi.org/10.1200/GO.20.00097
2. Dinmohamed AG. Fewer cancer diagnosis during the COVID-19 epidemic in the Netherlands. Lancet Oncol 2020; 750–751.
https://doi.org/10.1016/S1470-2045(20)30265-5
3. Hongyan Zhang LW. A Multicentre Study of Coronavirus Disease 2019 Outcomes of Cancer Patients in Wuhan, China.medRxiv 2020.03.21.20037127
4. Liang WGW. Cancer patients in SARS-CoV-2 infection: a nationwide analysis in China. Lancet Oncol 2020 Mar; 21(3): 335–337.
https://doi.org/10.1016/S1470-2045(20)30096-6
5. Matthew D, Tucker ALY. Severe-COVID-19 and mortality among patients (pts) with prostate cancer (PCa) receiving androgen deprivation therapy (ADT). Journal of Clinical Oncology 2021; 39 (Suppl 6): 39.
6. Montopoli MZ S-G. Androgen-deprivation therapies for prostate cancer and risk of infection by SARS-CoV-2: a population-based study (N = 4532). Ann Oncol 2020 Aug; 31(8): 1040–1045.
7. Wambier CG, GA-G. Androgen sensitivity gateway to COVID-19 disease severity. Drug Dev Res 2020 Nov; 81(7): 771–776.
https://doi.org/10.1002/ddr.21688