Report: Examination of microscopic haematuria (based on the Guideline of the American Urological Association)
DOI: 10.22591/magyurol.2024.1.villanyik.24
Authors:
Villányi Kinga dr.
Pécsi Tudományegyetem KK, Urológiai Klinika, Pécs (igazgató: Szántó Árpád dr.)
Summary
Macroscopic haematuria is one of the most common symptoms in outpatient and emergency departments, and always requires a detailed urological examination. Microhaematuria (MH), which is directly non-visible and is discovered by chance, can be an early sign of urological tumours. Patients represent a heterogeneous population regarding the risk of occurrence of urogenital malignancies.
The European Association of Urologists (EAU) has not published specific guidelines for the evaluation of haematuria. The presented 2020 AUA guideline recommends an individualized approach to the evaluation of microhaematuria (MH). The purpose of the directive is to optimize the examination of patients. The guideline establishes risk groups from the point of view of urogenital malignancy and recommends risk-adapted examinations.
LAPSZÁM: MAGYAR UROLÓGIA | 2024 | 36. ÉVFOLYAM, 1. SZÁM
Összefoglalás
A makroszkópos hematúria az egyik leggyakoribb tünet a járóbeteg- és sürgősségi osztályokon, mindig részletes urológiai kivizsgálást tesz szükségessé. A szemmel nem látható, véletlenszerűen felfedezett mikrohematúria (MH) az urológiai daganatok korai jele lehet. A betegek heterogén populációt képviselnek, közöttük az urogenitális rosszindulatú daganatok előfordulásának kockázata igen eltérő.
Az Európai Urológus Társaság (EAU) nem tett közzé konkrét irányelveket a hematúria értékelésére vonatkozóan. A bemutatott 2020-as AUA-irányelv egyénre szabott megközelítést javasol a mikrohematúria értékeléséhez, célja a mikrohematúriás betegek kivizsgálásának optimalizálása. Urogenitális rosszindulatú daganat szempontjából különböző kockázati csoportokat állapít meg és kockázatalapú kivizsgálást javasol.
A hematúria az egyik leggyakoribb urológiai diagnózis, az okok kivizsgálása az urológiai ellátások több mint 20%-át teszi ki. A mikrohematúriában szenvedő betegek heterogén populációt képviselnek, közöttük az urogenitális rosszindulatú daganatok előfordulásának kockázata igen eltérő. Egészséges önkéntesek körében a mikrohematúria (MH) előfordulási gyakoriságát 2,4%-31,1%. Húgyúti rosszindulatú daganat a vizsgált betegek mindössze 3%-ánál diagnosztizálható (2).
A betegspecifikus jellemzők lényegesen módosíthatják e daganatok kialakulásának kockázatát. Az Amerikai Urológus Társaság iránymutatása (2020) személyre szabott diagnosztikai stratégiát javasol (1).
Definíció
A klinikai definíció:
3 vagy több vörösvérsejt jelenléte látóterenként mikroszkópos vizsgálat során. MH nem diagnosztizálható csak dipstick teszt alapján. A dipstick teszt a peroxidáz-aktivitást méri, amit megzavarhatnak olyan tényezők, mint például a povidon-jód használata, a myoglobinuria és a kiszáradás (2).
Kivizsgálás
A kivizsgálás menetét az 1. ábra foglalja össze. Része a részletes anamnézisfelvétel különös tekintettel a prediszponáló faktorokra, valamint a részletes fizikális vizsgálat. A thrombocytaaggregáció-gátló vagy antikoaguláns gyógyszer szedése fontos tényező, de ezeket a betegeket is ugyanúgy kell értékelni, mint a nem antikoaguláltakat, mivel esetükben is hasonló a rosszindulatú daganat kockázata.
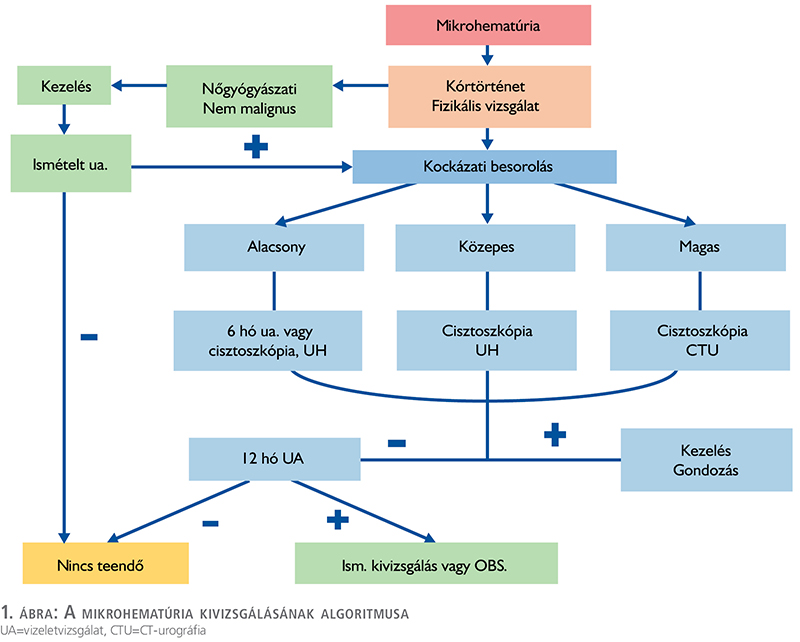
- Különösen fontos az urothelialis daganat (UC) kockázati tényezők felmérése:
- UC-megbetegedés a családban,
- irritatív alsó húgyúti tünetek,
- megelőző kismedencei besugárzás,
- megelőző cyclophosphamid, ifosfamid kemoterápiás kezelés,
- benzol vagy aromás aminexpozíció,
- krónikusan viselt húgyúti idegen test.
Az MH oka lehet nőgyógyászati és nem malignus urológiai eredet (pl. uroinfekció, kőbetegség). Ezek szanálása után ismételt vizeletvizsgálat szükséges a mikrohematúria megszűnése vagy megléte irányába. Ha az MH továbbra is fennáll, kockázatalapú urológiai értékelést és kivizsgálást kell végezni.
Proteinuria, dysmorf vvt-k jelenléte, veseelégtelenség esetén nefrológiai vizsgálat végzése is indokolt.
Kockázati besorolás
Az adatok alapján az MH-ban szenvedő betegeket urogenitális rosszindulatú daganat szempontjából alacsony, közepes vagy magas kockázati kategóriába soroljuk (1. táblázat).
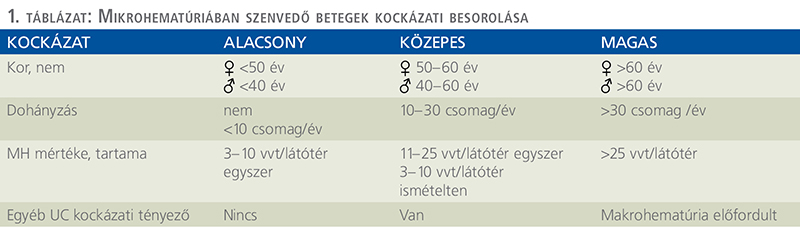
Az urothelialis carcinoma előfordulásának kockázatát <1%-ra becsülhetjük az alacsony kockázatúak, 1-2%-ra a közepes kockázatúak esetében, és 10%-ra vagy nagyobbra a magas kockázatú csoport esetében (3).
Endoszkópos és képalkotó vizsgálatok
A szükséges diagnosztikus vizsgálatok a cost-benefit arányt figyelembe véve az egyes kockázati kategóriákban eltérőek (2. táblázat).

Alacsony kockázat esetén invazivitása miatt a cisztoszkópia elvégzése mérlegelendő. A betegeket be kell vonni a döntéshozatalba, miszerint a hat hónapon belüli ismételt vizeletvizsgálatot vagy a cisztoszkópiát és a vese ultrahangvizsgálatát választják (4).
Azokat az alacsony kockázatú betegeket, akiknél nem végeznek cisztoszkópiát vagy felső húgyúti képalkotó vizsgálatot, és az ismételt vizeletvizsgálat során MH mutatható ki, át kell sorolni a közepes vagy magas kockázatú betegek közé.
Az MH hátterében leggyakrabban felfedezett urológiai malignitás a hólyagdaganat. Míg a képalkotó vizsgálatok szenzitivitása gyenge a hólyagrák azonosítására, a cisztoszkópia szenzitivitása 98% (5), ezért a cisztoszkópiát közepes kockázatú MH-betegeknél el kell végezni. A veseultrahang megfelelő érzékenységgel és specificitással rendelkezik a veseparenchyma-daganatokra, alacsonyabb költséggel és kisebb kockázattal jár (pl. ionizáló sugárzás, intravénás kontrasztreakciók és álpozitív eredmények), mint a kontrasztanyagos képalkotó vizsgálatok. Másrészt a veseultrahang szenzitivitása a felső traktus urothelialis carcinomája (UTUC) esetében gyenge (14%) (6). Negatív UH és cisztoszkópia ellenére perzisztáló vagy visszatérő MH esetén további képalkotó vizsgálatok (CT, MR) végezhetők.
Cisztoszkópiát és felső húgyúti képalkotó vizsgálatot kell végezni magas kockázatú MH-ban szenvedő betegeknél. Lehetőségek a felső húgyutak képalkotó vizsgálatára magas kockázatú betegeknél:
- ha nincs ellenjavallat kontrasztanyagos CT-urográfia választandó;
- ha a CT ellenjavallt (pl. veseelégtelenség, kontrasztanyag-allergia) MR-urográfia javasolt;
- ha egyik sem végezhető, retrográd pielográfia és nem kontrasztos CT- esetleg UH-vizsgálat szükséges.
Azoknál az MH-ban szenvedő betegeknél, akiknek a családjában előfordult vesesejtes karcinóma (RCC) vagy ismert genetikai eredetű vesetumor-szindróma (von Hippel–Lindau, Birt–Hogg–Dube, örökletes papilláris vesesejtes rák, örökletes leiomyomatosus vesesejtes rák, sclerosis tuberosa), a felső húgyutak képalkotó vizsgálatát el kell végezni a kockázati kategóriától függetlenül.
Nem javasolja a vizeletcitológia vagy a vizeletalapú tumormarkerek használatát az MH kezdeti értékelése során, szűrő jelleggel, mert a markervizsgálatok nem nyújtottak többletinformációt a cisztoszkópiához képest.
Az egyetlen terület, ahol a citológiának szerepe lehet, az in situ carcinoma (CIS) kimutatása. Javasolt elvégezni a perzisztáló MH-ban szenvedő betegek további kivizsgálása során, valamint azon a betegek esetében, akiknek irritatív tünetei, vagy egyéb CIS-re utaló kockázati tényezői vannak.
Nyomonkövetés
Negatív kivizsgálási eredmény esetén a vizeletvizsgálatot 12 hónapon belül ismételni szükséges. Amennyiben ennek eredménye is negatív, további urológiai gondozás nem szükséges.
Akiknél tartós, vagy visszatérő MH észlelhető, az MH progressziója jelentkezik, vagy új urológiai tünetek jelentkeznek, újbóli kivizsgálást kell kezdeményezni.
Irodalom
1. Barocas DA, Boorjian SA, Alvarez RD, et al. Microhematuria: AUA/SUFU guideline. J Urol 2020; 204: 778. https://doi.org/10.1097/JU.0000000000001297
2. Davis R, Jones JS, Barocas DA, et al. Diagnosis, evaluation and follow-up of asymptomatic microhematuria (AMH) in adults: AUA guideline. J Urol 2012; 188: 2473. https://doi.org/10.1016/j.juro.2012.09.078
3. Tan WS, Ahmad A, Feber A, et al. Development and validation of a haematuria cancer risk score to identify patients at risk of harbouring cancer. J Intern Med 2019; 285: 436. https://doi.org/10.1111/joim.12868
4. Georgieva MV, Wheeler SB, Erim D, et al. Comparison of the harms, advantages, and costs associated with alternative guidelines for the evaluation of hematuria. JAMA Intern Med 2019; 179: 1352.
https://doi.org/10.1001/jamainternmed.2019.2280
5. Blick CGT, Nazir SA, Mallett S, et al. Evaluation of diagnostic strategies for bladder cancer using computed tomography (CT) urography, flexible cystoscopy and voided urine cytology: results for 778 patients from a hospital haematuria clinic. BJU Int 2011; 110: 84.
https://doi.org/10.1111/j.1464-410X.2011.10664.x
6. Babjuk M, Böhle A, Burger M, et al. EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder: update 2016. Eur Urol 2017; 71: 447. https://doi.org/10.1016/j.eururo.2016.05.041