Our experience with MRI – ultrasound fusion prostate biopsy at Uzsoki Street Hospital
DOI: 10.22591/magyurol.2025.1.horvathl.15
Authors:
Horváth László dr.1, Tóth Zoltán dr.1, Zolcsák Attila dr.1, Kátai Tamás Zoltán dr.2
1Uzsoki Utcai Kórház, Urológiai Sebészeti Osztály, Budapest (osztályvezető: Tóth Zoltán dr.)
2Uzsoki Utcai Kórház, Központi Röntgen Diagnosztika, Budapest (osztályvezető: Egyed Zsófia dr.)
Summary
Introduction: Prostate cancer (PCa) is the second most common cancer among men. After the routine PSA blood sampling and rectal digital examination the histological sampling is the standard method of the final diagnosis.
Usually, the conventional map biopsy is used, but nowadays it is possible to perform a transrectal ultrasound guided MRI fusion biopsy of suspicious lesions.
Patients and methods: At the Urology Department of the Uzsoki Street Hospital, 77 ultrasound guided MRI fusion biopsy cases were performed between May 2020 and March 2023. Patients with suspected prostate cancer were selected randomly based on the regional duty of care.
Results: From the 55 biopsy naive patients, 42 were confirmed to have prostate cancer, 28 (51%) with clinically significant grade >ISUP1. From the 22 patients who underwent previous biopsy, 14 were confirmed to have PCa, 8 (36%) >ISUP1.
In 14% of all patients, 19.5% of all positive results, prostate cancer was detected only by MR fusion biopsy, 6 cases >ISUP1 grade.
Conclusion: Transrectal ultrasound guided MRI fusion biopsy is considered an indispensable diagnostic modality in the routine urological practice, and can be performed with the same time as the convection biopsy in an outpatient setting with a similar complication rate. There were no significant differences between radiology departments.
LAPSZÁM: MAGYAR UROLÓGIA | 2025 | 37. ÉVFOLYAM, 1. SZÁM
Összefoglalás
Bevezetés: A prosztatarák (PCa) a második leggyakoribb daganatos megbetegedés a férfiak körében. A rutinszerűen alkalmazott PSA-vérvétel és rektális digitális vizsgálat mellett felállított gyanú alapján a szövettani mintavétel jelenti a diagnosztizálás standard módszerét. Általában a hagyományos térképbiopszia módszerével történik a mintavétel, azonban napjainkban már lehetőség van egy MR-vizsgálat során gyanúsnak véleményezett terület UH-vezérelt, MR fúziós biopsziájára is.
Betegek és módszer: Az Uzsoki Utcai Kórház Urológiai Osztályán 2020. május és 2023. március között 77 esetben végeztünk UH-vezérelt MR fúziós biopsziát. A prosztatatarák-gyanús betegek kiválasztása területi ellátási kötelezettség alapján, random módon történt.
Eredmények: 55 biopszianaiv páciensből 42-nél igazolódott prosztatatarák, 28 esetben (51%) klinikailag szignifikáns, ISUP 1-et meghaladó grádusú. 22 korábbi biopszián átesett betegekből 14-nél igazolódott PCa, 8 esetben (36%) >ISUP1.
Az összes beteg 14%-ánál, az összes pozitív eredmény 19,5%-ánál csak az MR fúziós mintavétellel került felismerésre a prosztatadaganat, 6 esetben >ISUP1 stádiumban.
Következtetés: Az UH-vezérelt MR fúziós biopszia a mindennapi urológiai gyakorlatban elengedhetetlen diagnosztikus módszernek tekinthető, a konvencionális biopsziával gyakorlatilag megegyező idő alatt, ambuláns keretek között is elvégezhető hasonló szövődményrátával. Az egyes radiológiai osztályok leletei között érdemi különbség nem mutatkozott.
Bevezetés
A prosztatarák (prostate cancer – PCa) a második leggyakoribb daganatos megbetegedés a férfiak körében, világszerte mintegy 1,4 millió új eset kerül diagnosztizálásra (2020) évente (1, 2).
30 éves kor alatt a prevalencia 5% alatti, míg 79 éves kor felett elérheti az 59%-ot is (3). Magyarországon a Nemzeti Rákregiszter adatbázisa szerint 2020-ban 3691 új eset került felfedezésre (30 éves kor alatt 0, 79 éves kor felett 470), a férfiak körében a harmadik leggyakoribb rosszindulatú daganatos megbetegedés volt (4).
Korábban, a prosztataspecifikus-antigén (PSA) felfedezése, mindennapi használata előtt elsősorban csontáttétek esetén merült fel a prosztatadaganat gyanúja (5). Napjainkban az 50 év feletti férfiak ajánlott éves prosztatavizsgálata (rektális digitális vizsgálat – RDV) és PSA-vérvétel ad módot a korai felismerésre (6). Ezen vizsgálatok mellett a képalkotó diagnosztika fejlődésével lehetőség nyílt a prosztata mágneses rezonancia (prosztata MR) képalkotó vizsgálatára, amely további támpontot ad a prosztatarák diagnózisához vezető úton.
A fent említett vizsgálatokkal alapos gyanú merülhet fel a daganatos elváltozásra, azonban az egyetlen biztos kimutatási módszert a mai napig a prosztatából történő szövettani mintavétel (biopszia) jelenti. Fontos kiemelni, hogy míg a non-invazív vizsgálatok érdemi szövődmények nélkül végezhetőek, a prosztatabiopszia kivitelezése ezzel szemben nagyobb kockázattal jár. A lehetséges szövődmények (vizeletelakadás [3%], végbélvérzés [3,4%], vérvizelés [53,4%], prosztatagyulladás [3%]) miatt csak gondos kivizsgálást követően ajánlott a beavatkozást elvégezni (7). Fontos cél tehát a mihamarabbi lehető legpontosabb diagnózis felállítása, amellyel a felesleges biopsziák száma csökkenthető.
Prosztatadaganat gyanúja a kóros tapintási lelet, az emelkedett PSA-szint, a PSA-ból és a prosztata méretéből számított érték, a PSA-denzitás (PSA-D), valamint a kóros MR-lelet alapján állítható fel. Ezen vizsgálati eredményeket összesítve döntünk a biopszia elvégzése vagy mellőzése mellett.
A prosztatabiopszia hagyományos módja a térképbiopszia, amely során a prosztatából – előre meghatározott rendszer szerint – minimum 12 darab mintavétel történik. A beavatkozás történhet a gáton és a végbélen keresztül is. A technika fejlődése és a megfelelő kritériumrendszer kialakulása napjainkban lehetővé teszi a térképbiopszia mellett a célzott biopsziás mintavételt is, amely az MR-vizsgálaton gyanúsnak minősített területből történik.
A gyanú felállítása a PI-RADS (Prostate Imaging-Reporting and Data System) kritériumrendszer alapján történik. Egytől ötig terjedő skálán megkülönböztetünk nagyon valószínűtlen (PI-RADS 1), valószínűtlen (PI-RADS 2), közepesen gyanús (PI-RADS 3), gyanús (PI-RADS 4) és nagyon gyanús (PI-RADS 5) elváltozásokat (8). A fentiek esetében a klinikailag szignifikáns PCa prevalenciája PI-RADS 1-2 esetén 6%, PI-RADS 3 esetén 16%, PI-RADS 4-5 esetén 62% (9).
Betegek és módszerek
Az Uzsoki Utcai Kórház Urológiai Osztályán a prosztatabiopsziák legnagyobb részét transrectalisan végezzük ultrahang- (UH) vezérelten, 2020 előtt csak térképbiopsziát végeztünk. 2020.05.06. – 2023.03.30. között 77 esetben lehetőségünk nyílt UH-vezérelt MR fúziós biopszia végzésére.
A prosztatadaganat-gyanús betegek kiválasztása random módon történt, területi ellátási kötelezettség alapján. A betegpopuláció alapadatait az 1. táblázat foglalja össze.
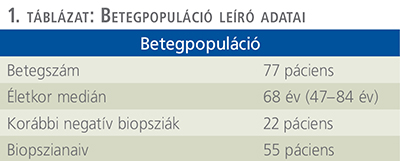
Az MR fúziós biopsziára kerülő páciensek megelőző vizsgálati eredményei közül az emelkedett PSA-érték, a növekedett prosztatatérfogat (medián érték: 52 ml), valamint az esetek több mint egyharmadában a pozitív tapintási lelet volt kiemelhető. A vizsgált betegpopuláció medián PSA denzitása az európai irányelvek szerint a középmagas rizikócsoportba esett. Ezen adatokat a 2. táblázat foglalja össze.
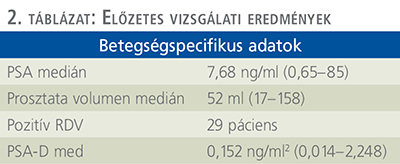
Az MR-vizsgálatokat 39 alkalommal a területileg illetékes MR-laborokban végezték el, 38 esetben az Uzsoki Utcai Kórházban.
A használt MR-felvételek megfeleltek az aktuális PI-RADS szerinti kritériumoknak. A felvételeket kórházunk tapasztalt radiológusával áttekintve jelöltük ki a célzott biopsziás területeket. A képanyagokat külső adathordozókról (CD, pendrive) töltöttük be.
A beavatkozásokat egy GE Logic S8 Ultrahanggal és a hozzá tartozó navigációs rendszerrel végeztük, amelyet a készülék magyarországi forgalmazója helyezett el osztályunkon. A beavatkozások során radiológus kolléga nem volt jelen. A célzott területek kijelölését, a navigációs rendszer beállítását, valamint a mintavételt is urológus végezte. Az összes biopsziát járóbeteg-ellátás keretében végeztük, a mintavételhez Bard MN1820 Magnum™ 18 G × 20 cm biopsziás tűt és Bard Magnum™ biopsziás pisztolyt használtunk (3–5. táblázat).
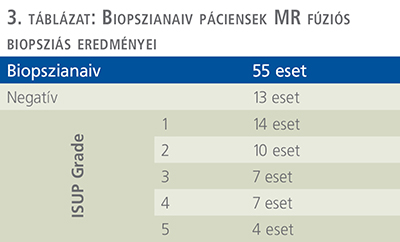
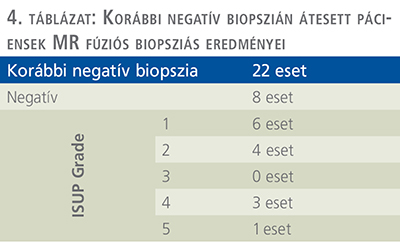
A mintavétel előtt a betegek antibiotikumprofilaxisban nem részesültek, a beavatkozásra povidon-jód hatóanyagú kúp rektális felhelyezése után 4 órával került sor. Narkózist a biopsziák során nem alkalmaztunk. Tekintettel arra, hogy tapasztalataink szerint a helyi Lidocain hatóanyagú érzéstelenítési procedúra a betegek számára több szubjektív panaszt okozott, mint amennyi kedvező hatása volt, így ezt is csak az esetek elenyésző hányadánál alkalmaztuk.
A pácienseket a bal oldalukra, térdüket a mellkasuk felé húzva, jobb kézzel a vizsgáló ágy szélébe kapaszkodva, stabil pozícióba fektettük, majd a jobb oldali csípő felett elhelyeztük a navigációhoz szükséges mágneses érzékelő egységet. Braunol-oldattal való lemosást követően az izolált rektális ultrahang-transzducert és a hozzá csatlakoztatott tűvezetőt a végbélbe vezettük.
Az ultrahangon betöltött MR-vizsgálati képanyagok közül a T2 axiális felvételeket alkalmaztunk. Egy jelölő segítségével az MR-szeleteken kijelöltük a PI-RADS kritériumok szerint gyanús egy, vagy több elváltozást, majd kiválasztottuk a prosztata apex és a húgycső átmenetet tartalmazó szeletet, amelyeken már a levator izomzat is jól látható volt. Az ultrahangon is beállítottuk ugyanezt a területet, amelyben legnagyobb támpontnak a húgycső kezdeti szakasza és a levator izmok MR-képekhez hasonló morfológiája bizonyult. Az egyező helyzet megtalálása után a „Lock” gomb megnyomásával az MR- és az UH-képet rögzítettük egymáshoz. Ezután az UH-fej mozgatásával az MR-síkok is változtak; a korábban az MR-en kijelölt pontok megjelentek az UH-képernyőn is (1. és 2. ábra).
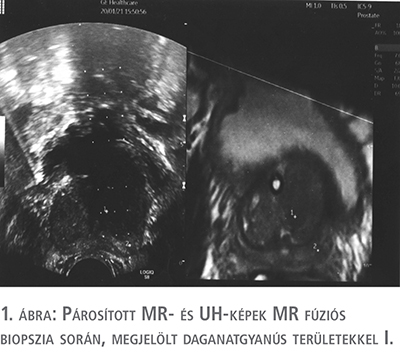
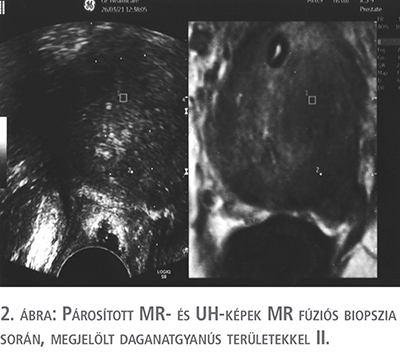
Először a fúziós mintavételeket végeztük el (minden gyanús elváltozásból 2-2 szövetminta), majd a navigációs rendszer kikapcsolása után térképbiopsziát is végeztünk. Rövid ambuláns obszerváció után otthonukba bocsátottuk a betegeket.
Kezdetben egy mintavétel elvégzése körülbelül 40-45 percet vett igénybe. A kezdeti tanulási időszak (kb. 30 elvégzett biopszia) után ez az idő átlagosan 15-20 percre csökkent.
Eredmények
Az adatok elemzésekor megkülönböztettünk korábbi biopszián átesett és biopszianaiv betegeket.
55 biopszianaiv páciensből 42-nél igazolódott prosztatatarák (PCa), 28 esetben (51%) klinikailag szignifikáns, ISUP (International Society of Urological Pathologists) 1-et meghaladó stádiumban (>ISUP 1).
22 korábbi biopszián átesett betegből 14-nél igazolódott PCa, 8 esetben (36%) >ISUP 1.
Az MR fúziós biopszia fontosságát igazolja, hogy az elvégzett 77 UH-vezérelt MR fúziós prosztataminta-vételből 11 páciensnél, vagyis az összes beteg 14%-ánál, az összes pozitív eredmény 19,5%-ánál csak az MR fúziós mintavétel alapján igazolódott prosztatadaganat, 6 esetben >ISUP 1.
28 (20 >ISUP 1) esetben az MR fúziós és a térképbiopsziából is prosztatadaganat igazolódott, amelyek közül 5 esetben az MR fúziós bioptátum magasabb, 17 esetben azonos és 6 esetben alacsonyabb ISUP graddel rendelkezett.
A 77 biopszia során 5 esetben észleltünk szövődményt: 1 páciensnél (1,3%) prosztatagyulladást, 1 páciensnél (1,3%) hólyaggyulladást és 3 páciens (3,9%) esetében vérvizelést. A panaszok az észlelés után alkalmazott megfelelő kezelés mellett szanálódtak.
A tapintási lelet korlátozott értékére hívja fel a figyelmet, hogy azon 48 beteg közül, akiknél a tapintási lelet negatívnak bizonyult, 30-nál (63%) igazolódott prosztatadaganat, 15 esetben (31%) klinikailag szignifikáns, ISUP 1-et meghaladó stádiumban.
29 pozitív tapintási leletű betegből 25-nél (86%) került diagnosztizálásra PCa, 20 esetben (67%) ISUP 1 feletti stádiumban.
4 alatti PSA-értékkel 9 biopsziát végeztünk, 6 esetben igazolódott prosztatadaganat, 5 esetben ISUP 1-et meghaladó stádiumban.
Következtetések
Eredményeink összegzésénél törekedtünk több aspektust is megvizsgálni.
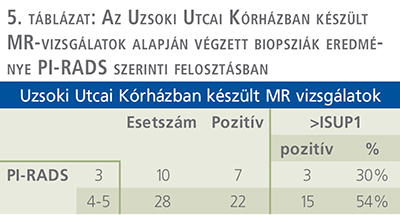
Összevetettük a saját és az egyéb intézményekben készült MR-vizsgálatok alapján készült biopsziák eredményességét. Az Uzsoki Utcai Kórházban készült MR-vizsgálatok esetén leírt PI-RADS 3 léziókból vett mintákból 30%-ban igazolódott szignifikáns prosztatadaganat, míg PI-RADS 4-5 léziók esetén 54%-ban.
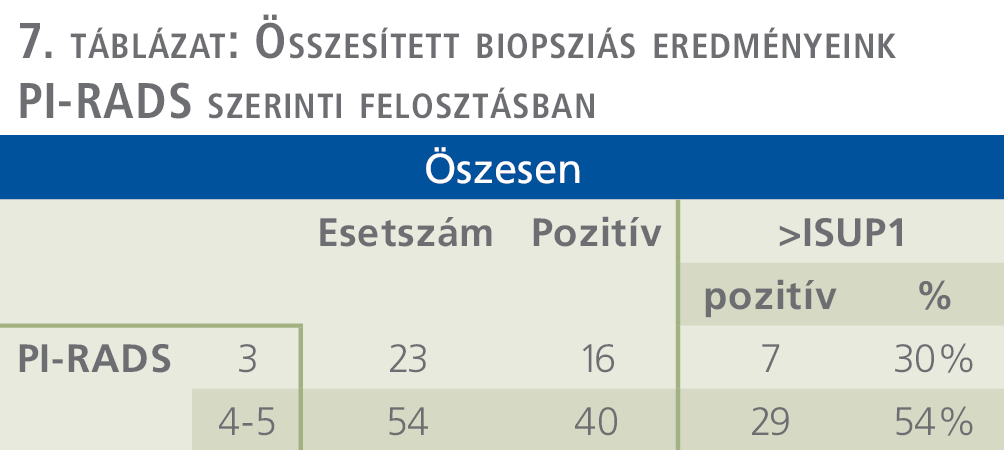
Más intézményekben készült MR-vizsgálatok esetén érdemi különbséget nem tapasztaltunk, PI-RADS 3 léziók esetén 31%-ban, PI-RADS 4-5 léziók esetén 54%-ban igazolódott ISUP 1 stádiumot meghaladó prosztatadaganat. A fenti eredményeket az 5., 6., 7. táblázat foglalja össze.
Az osztályunkon végzett UH-vezérelt MR fúziós biopsziák eredményessége megfeleltethető a nemzetközi irodalomban olvasható PI-RADS szerinti PCa prevalencia adatoknak.

Az UH-vezérelt MR fúziós prosztatabiopszia elengedhetetlen lenne a mindennapi urológiai gyakorlatban. Alkalmazásával csökkenthető az elvégzett biopsziák száma, valamint olyan kezelést igénylő proszatatadaganatok igazolhatók, amelyek a hagyományos térképbiopsziás módszerrel nem minden esetben.
A beavatkozás radiológus jelenléte nélkül is végezhető. Kezdeti tanulási időszak után a konvecionális biopsziával összeegyeztethető idő alatt, ambuláns keretek között is elvégezhető diagnosztikus módszer. Szövődmények számában a hagyományos biopsziánál tapasztaltakkal gyakorlatilag megegyezik.
Remélhetőleg a közeljövőben az eljárási mód minden prosztatabiopsziára kerülő beteg esetében elérhetővé válik.
Irodalom
1. Culp MB, Soerjomataram I, Efstathiou JA, et al. Recent Global Patterns in Prostate Cancer Incidence and Mortality Rates. Eur Urol 2020; 77: 38–52. https://doi.org/10.1016/j.eururo.2019.11.030
2. Ferlay J, Ervik M, Lam F, et al. IARC. WHO. Data visualization tools for exploring the global cancer burden in 2020. 2022.
https://gco.iarc.fr/today/home
3. Bell KJ, Del Mar C, Wright G, et al. Prevalence of incidental prostate cancer: A systematic review of autopsy studies. Int J Cancer 2015; 137: 1749–57. https://doi.org/10.1002/ijc.29538
4. Kenessey I, Dobozi M, Kiss É, és mtsai. Nemzeti Rákregiszter. 2024. www.oncol.hu/nemzeti-rakregiszter/
5. Denmeade SR, Isaacs JT. A history of prostate cancer treatment. Nat Rev Cancer 2002; 2: 389–96. https://doi.org/10.1038/nrc801
6. Tenke P, Horti J, Balint P, et al. Prostate cancer screening. Recent Results Cancer Res 2007; 175: 65–81. https://doi.org/10.1007/978-3-540-40901-4_5
7. Wegelin O, Exterkate L, van der Leest M, et al. Complications and Adverse Events of Three Magnetic Resonance Imaging-based Target Biopsy Techniques in the Diagnosis of Prostate Cancer Among Men with Prior Negative Biopsies: Results from the FUTURE Trial, a Multicentre Randomised Controlled Trial. Eur Urol Oncol 2019; 2: 617–624. https://doi.org/10.1016/j.euo.2019.08.007
8. Scott R, Misser SK, Cioni D, et al. PI-RADS v2.1: What has changed and how to report. SA J Radiol 2021; 25: 2062.
https://doi.org/10.4102/sajr.v25i1.2062
9. Schoots IG, Padhani AR. Risk-adapted biopsy decision based on prostate magnetic resonance imaging and prostate-specific antigen density for enhanced biopsy avoidance in first prostate cancer diagnostic evaluation. BJU Int 2021; 127: 175–178. https://doi.org/10.1111/bju.15277