Bladder augmentation with continent stoma formation in case of a urological and gynaecological complex congenital developmental disorders
DOI: 10.22591/magyurol.2025.1.reparukj.22
Authors:
Repáruk József dr.1, Majoros Attila dr.2, Keszthelyi Attila dr.2
1Zala Vármegyei Szt. Rafael Kórház, Urológiai Osztály, Veszprém (osztályvezető: Kozma-Bognár Tamás dr.)
2Semmelweis Egyetem, Urológiai Klinika és Uroonkológiai Centrum, Budapest (igazgató: Nyirády Péter dr.)
Summary
Introduction: Bladder exstrophy is a congenital developmental anomaly recognized at birth, often associated with abnormalities in other organs. Early reconstruction is essential; however, nearly half of the patients who undergo surgery may later experience urological and/or fertility complications. One such complication is neurogenic bladder dysfunction. While less invasive treatments exist, bladder augmentation is more frequently chosen in younger patients for its more durable outcomes.
Case report: A 24-year-old female patient presented at the Semmelweis University Urology Clinic with complaints of complete incontinence. Her medical history included multiple developmental anomalies: bladder exstrophy, epispadias, sphincter insufficiency, renal agenesis, vaginal duplex, uterus bicornis, rudimentary appendix, late-closing foramen ovale, complex morphological abnormalities of the spine and pelvic bones, and supernumerary fingers. She underwent multi-stage reconstructive surgery during childhood. Urodynamic studies confirmed reduced bladder capacity, detrusor hyperactivity, and sphincter insufficiency. The treatment plan included bladder augmentation and the creation of a catheterizable continent abdominal stoma. The patient’s rudimentary appendix was unsuitable for creating a Mitrofanoff stoma. Therefore, after bladder augmentation, a catheterizable urinary stoma was created from the oral end of the isolated ileal segment. The surgery was complication-free and resolved her urological dysfunctions, although reconstruction of the gynaecological organs remains pending.
Conclusions: In cases of neurogenic lower urinary tract dysfunction arising from bladder exstrophy, bladder augmentation using an isolated intestinal segment and the creation of a catheterizable continent abdominal stoma is a viable and effective treatment option, especially for younger patients.
LAPSZÁM: MAGYAR UROLÓGIA | 2025 | 37. ÉVFOLYAM, 1. SZÁM
Összefoglalás
Bevezetés: A húgyhólyag-extrophia születéskor felismert fejlődési rendellenesség, amely gyakran társul egyéb szervek eltéréseivel. Az állapot mielőbbi rekonstrukciót kíván, azonban a műtéten átesett páciensek közel felénél várható későbbiekben urológiai- és/vagy fertilitási szövődmény. Egyik ilyen a neurogén húgyhólyag-diszfunkció. Kezelésére bár kevésbé invazív eljárások is léteznek, fiatalkorban gyakrabban választják a tartósabb eredmény reményében a húgyhólyag-augmentációt.
Esetismertetés: A Semmelweis Egyetem Urológia Klinikáján jelentkezett 24 éves nőbeteg teljes inkontinencia panaszával. Kórelőzményében többszörös fejlődési rendellenesség szerepelt: húgyhólyag-extrophia, epispadiasis, sphincter-elégtelenség, veseagenesia, vagina duplex, uterus bicornis, csökevényes appendix, későn záródó foramen ovale, gerinc- és medencecsontok komplex morfológiai zavara, valamint számfeletti kézujj. Gyermekkorában többlépcsős rekonstrukciós műtétet végeztek. Urodinámiás vizsgálattal csökkent húgyhólyag-kapacitás, detrusor hiperaktivitás és sphincter-elégtelenség igazolódott. Kezelési tervként a húgyhólyag-augmentáció és katéterezhető hasfali kontinens sztóma kialakítása mellett döntöttek. A beteg csökevényes appendixe Mitrofanoff-sztóma létrehozására alkalmatlan volt. Így a húgyhólyag-augmentációját követően a kirekesztett ileumszakasz orális végéből készítettek katéterezhető vizeletes sztómát. Szövődménymentes műtét segítségével az urológiai funkciózavart megoldották, azonban a nőgyógyászati szervek rekonsturkciója még hátra van.
Következtetések: Húgyhólyag-extrophia talaján kialakult neurogén alsó húgyúti funkciózavar esetén, a húgyhólyag kirekesztett bélszakasszal történő augmentációja és katéterezhető hasfali kontinens sztóma készítése jó eredményt biztosító, választható módszer főként fiatal betegeknél.
Bevezetés
Korábban önálló entitásként tárgyalt húgyhólyag-extrophia, ma már a húgyhólyag-extrophia-epispadiasis komplex részét képezi. A közös csoportba osztás okát, a megegyező etiológiai háttér: az intrauterin fejlődés során jelentkező cloacamembrán felszívódási zavara jelenti. Az eltérő klinikai megjelenési formák valójában ugyanannak a fejődési rendellenességnek eltérő spektrumú manifesztációi (1).
A húgyhólyag-extrophia gyakoriságát az irodalom nagy szórással említi. Az Egyesült Államokban élveszületésekre kb. 1:30 000 és 1:50 000 közötti gyakoriságra becsülik előfordulását, azonban az országon belüli adatok is nagy szórást mutatnak. Közép-európai becsült adatok közel hasonló gyakoriságot mutatnak, 3,3:100 000 és 10:100 000 között élveszülésenként. Az állapot férfiaknál gyakoribb, de ennek mértéke is széles intervallumban mozog. A férfi:nő arány 2,3:1 és 10:1 között szerepel az irodalomban (2).
A húgyhólyag-extrophia mind esztétika, mind funkcionális szempontból mielőbbi megoldást kívánó állapot. A külvilág felé hasfali defektuson keresztül nyitott húgyhólyag a visszatérő húgyúti fertőzések kapcsán potenciális veszélyt jelent a felső húgyutak károsodása szempontjából. A szakirodalom mihamarabb elvégzett hasfali és hólyagfali defektus zárást javasol. Ennek módjáról (egy, vagy több lépcsőben elvégzett), illetve időpontjáról (szülési időponthoz számítva azonnali vagy halasztott műtét) konszenzus nincs. Az eltérő megoldást preferáló intézmények eredményeit összehasonlítva, semmi féle előnyt vagy hátrányt nem sikerült kimutatni a különböző műtéti módszerek között (2). Sajnálatosan egyik megoldás sem kecsegtet jobb funkcionális eredménnyel vagy kevesebb késői szövődménnyel. Ez a tény kiemelendő, hiszen az esetek közel 50%-ánál várható korai felnőttkorban urogenitális szövődmény, amely gyakran orvosi beavatkozást igényel. Urológia szempontból külön említendő a neurogén alsó húgyúti diszfunkció, régi nevén „neurogén hólyag” kialakulása. Ez a progresszív elváltozás ugyanis a felső húgyutak irreverzibilis funkció romlását, korai veseelégtelenséget okozhat, nem beszélve a beteg életminőségének jelentős csökkenését okozó alsó húgyúti panaszokról (vizeletinkontinencia, vizeletretenció) (3).
Esetismertetés
A Semmelweis Egyetem Szülészeti és Nőgyógyászati Klinikáján jelentkezett egy 24 éves fiatal nőbeteg, aki többszörös fejlődési rendellenesség miatt coitusra alkalmatlan vaginalis deformitással élt.
Anamnézisében számfeletti kézujjak, hasfali- és húgyhólyag-defektus zárása valamint kétoldali lágyéksérv miatt csecsemőkorban összesen négy alkalommal elvégzett műtétek szerepeltek. Többszörös csigolyafejlődési rendellenesség és bordahiány miatt ortopédiai gondozásban részesült. Majd 16 éves koráig rendszeres orvosi kontroll alatt állt pitvari szeptumdefektus és bal oldali szoliter vese miatt. Ezt követően a beteg az orvosi látótérből eltűnt.
Bár a hölgynek genitális deformitása okozta fő panaszát, a szülész-nőgyógyász munkatárs alapos kivizsgálása kapcsán többek között többszörös urogenitális fejlődési rendellenesség igazolódott. Emellett a betegnél teljes vizeletinkontinencia is fennállt, nem érzett vizelési ingert, vizelete folyamatosan elszivárgott. A nőgyógyászati rekonstrukciós műtétet megelőzően urológiai konzílium kapcsán került a Semmelweis Egyetem Urológia Klinikája látóterébe a beteg. Komplex, urológiai- és urodinamikai vizsgálatot valamint MRI-képalkotást is magába foglaló kivizsgálás történt.
Korábbi hasi ultrahangleletben megtartott parenchymájú, üregrendszeri tágulattól mentes, bal oldali szoliter vesén és balra deviáló uteruson kívül egyéb kóros eltérés nem szerepelt. Azonban a húgyhólyagról biztonságban nem nyilatkoztak, leírás alapján „a húgyhólyag csak sejthető, benne sávszerű vizelet ábrázolódik”.
Teljes has és medence MRI-vizsgálat során az ép szerkezetű bal oldali szoliter vese mellett, ép tágasságú bal oldali urétert, a gyermekkorban primeren zárt húgyhólyagból ventrálisan, a hasfalra vezető fisztulajáratot, két egymástól teljesen különálló uterust és ezek folytatásában két, szintén teljesen különálló vaginát, ép ováriumokat valamint symphisisben nem egyesülő os pubisokat igazolt.
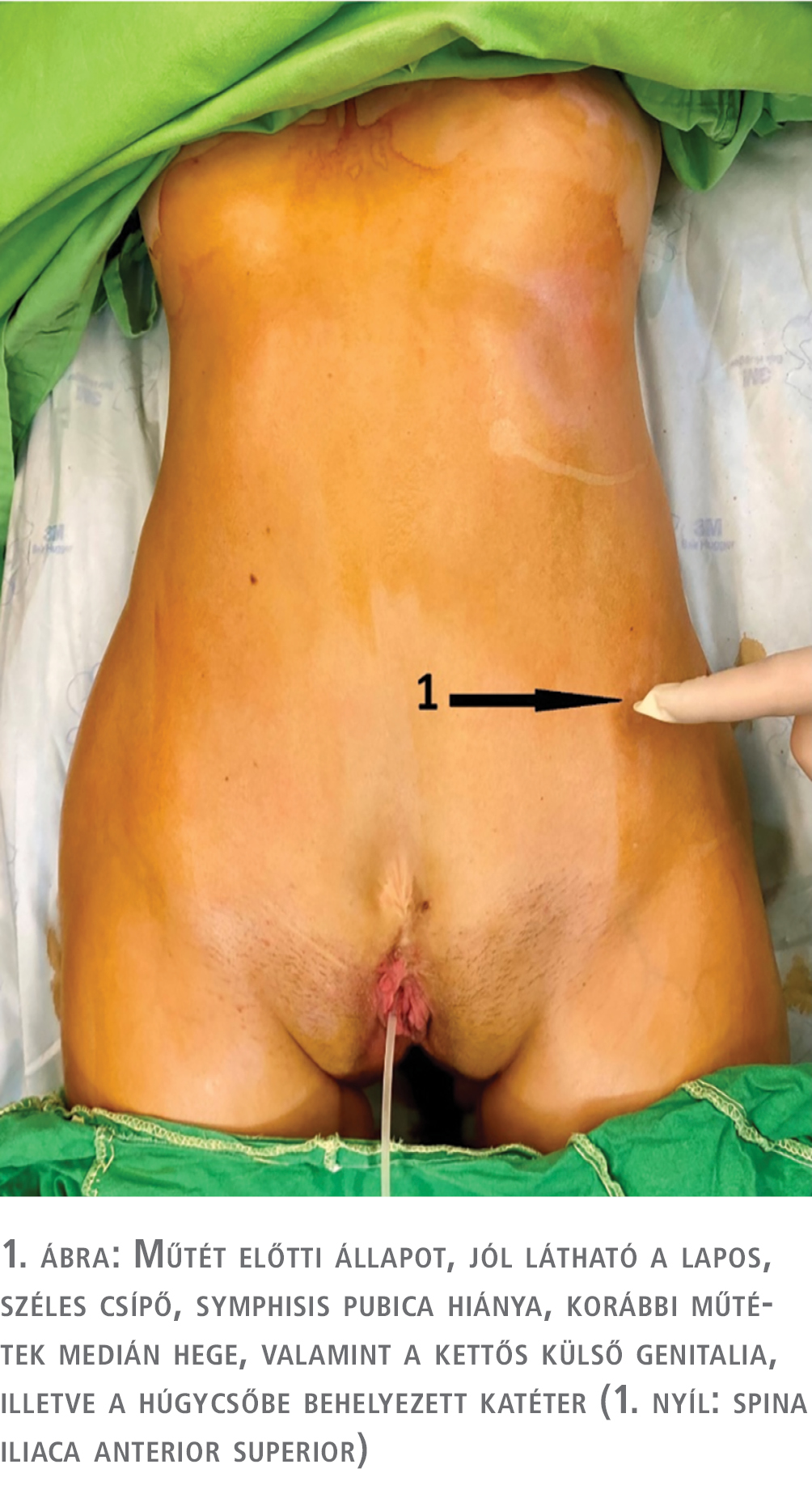
Fizikális vizsgálat során elsőként feltűnő elváltozások a markánsan széttartó medencecsontok, symphysis pubica hiány, kifelé rotált alsó végtagok, gyermekkorban elvégzett hasfali műtét hege valamint köldök hiánya voltak. Genitális régióban anteponált két egymástól független hüvelybemenet valamint anteponált végbélnyílás volt látható. A szeméremajkak nem fuzionáltak commissura anteriorban, a clitoris egyértelműen nem volt azonosítható. A szeméremajkaktól cranial felé a húgycsőnyílást a belőle folyamatosan szivárgó vizelet alapján lehetett csak azonosítani, szűkülete miatt csupán vékony PVC-katétert sikerült bevezetnünk.
A beteg laborparamétereiben jelentős eltérést nem észleltünk.
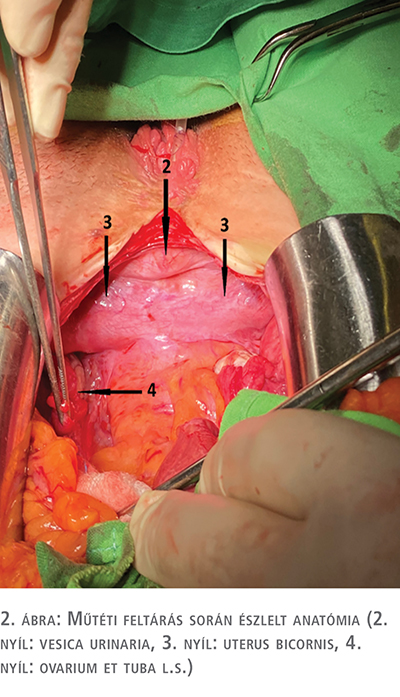
Anamnézis valamint fenti vizsgálatok alapján komplex, több szervrendszert érintő fejlődési rendellenesség igazolódott (1. és 2. ábra), amelyek:
- Későn záródó foramen ovale.
- Számfeletti kézujj.
- Húgyhólyag-extrophia.
- Epispadiasis.
- Osztott külső genitáliák.
- Nem fuzionáló kis és nagy ajkak.
- Vagina duplex.
- Uterus bicornis.
- Symphysis pubica hiánya.
- Két sacralis csigolya hiánya és bal oldali bordahiány.
- Jobb oldali veseagenesia.
Urodinamikai vizsgálat detrusor hiperaktivitást, alacsony hólyagkapacitást, magas intravesicalis nyomást, csökkent compliance-t és a húgycsőzáró sphincter elégtelenségét igazolta (vizeletretenció nem volt), amelyek alapján a betegnél kimondható volt a neurogén alsó húgyúti- diszfunkció diagnózisa. Az irodalom több lehetőséget is javasol neurogén alsó húgyúti-diszfunkció kezelésére, mint gyógyszeres terápia, intravesicalis Botox injekció valamint intermittálló önkatéterezés (4). Anticholinerg gyógyszeres kezelés kezdődött, amely várhatóan nem vezetett eredményre, majd ezt követően a húgyhólyag tárolási kapacitásának növekedését, intravesicalis nyomásának csökkenését és a vizeletkontinenciát is biztosító tartósabb eredményt és jobb életminőséget ígérő műtéti megoldást választottunk, amely a húgyhólyag kirekesztett vékonybélszakasszal történő augmentációját és katéterezhető sztóma (appendix sztóma) kialakítását valamint a külső húgycsőnyílás zárását jelentette.
A húgyhólyag megnyitásakor gomblyukszerű uréterszájadék tárult elénk, amely a magas nyomású húgyhólyag tartósabb fennállásának bizonyítéka. A betegnél egyidejűleg fennálló sphincter-elégtelenség, feltehetőleg „védő funkcióval” bírt a jelentősebb vesefunkció romlással szemben. Az intraoperativ diagnosztizált mindössze néhány milliméter hosszúságú, csökevényes appendix vermiformis nem tette lehetővé Mitrofanoff-sztóma kialakítását (3. ábra).
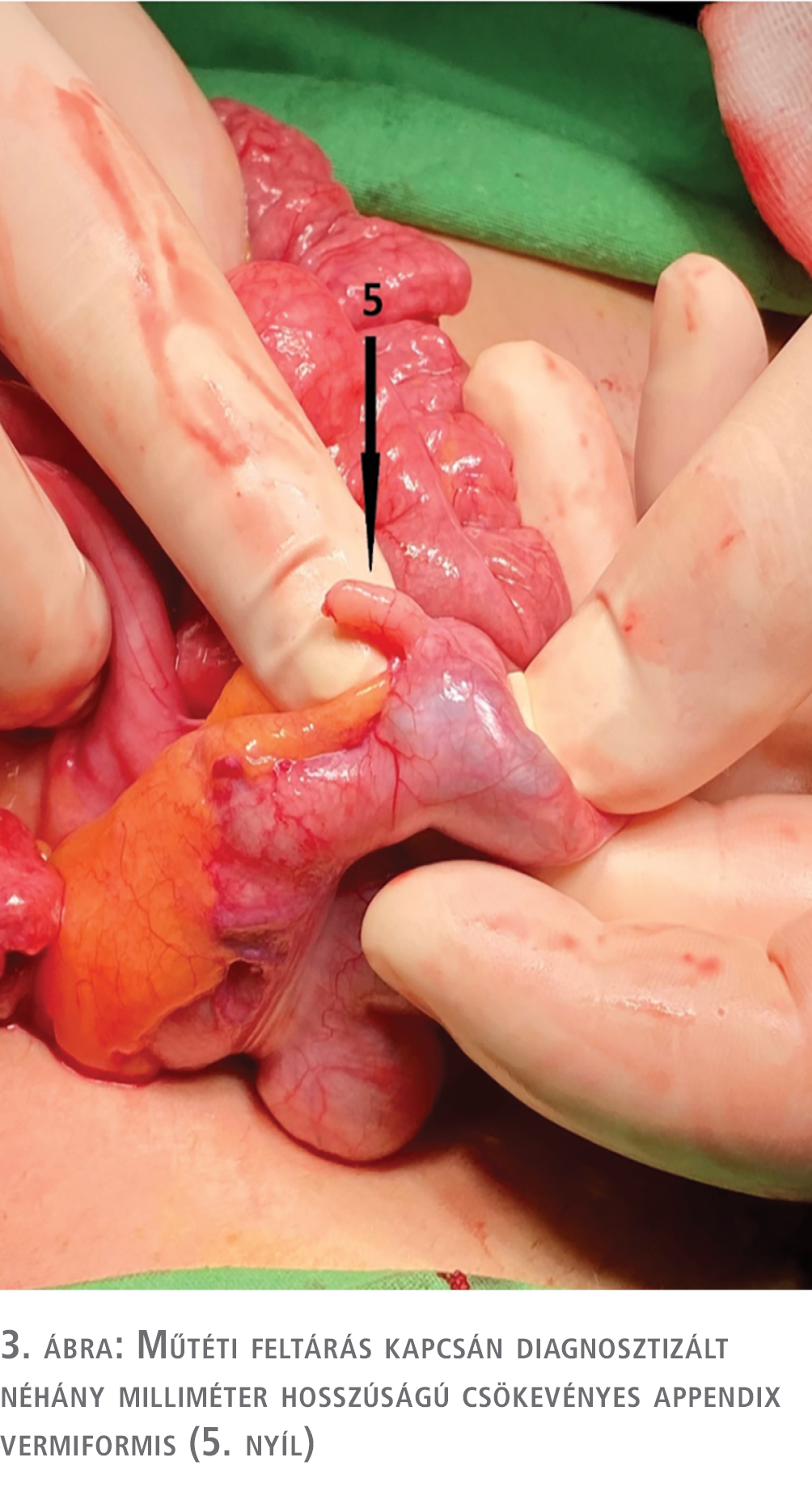
Így mind a hólyag-augmentációhoz, mind pedig a katéterezhető sztóma kialakításához ugyanazt a 40 cm-es reszekált terminális ileumszakaszt használtuk fel. A reszekált bélszakasz orális 7 cm-ét nem hasítottuk fel az anti-mesenterialis oldalán, lumenét raffolással beszűkítettük. Később ebből készítettük el a katéterezhető sztómát. A disztális felhasított ileumszakaszt félgömbbé hajtogatva szélesen anasztomizáltuk a húgyhólyaghoz (4. ábra).
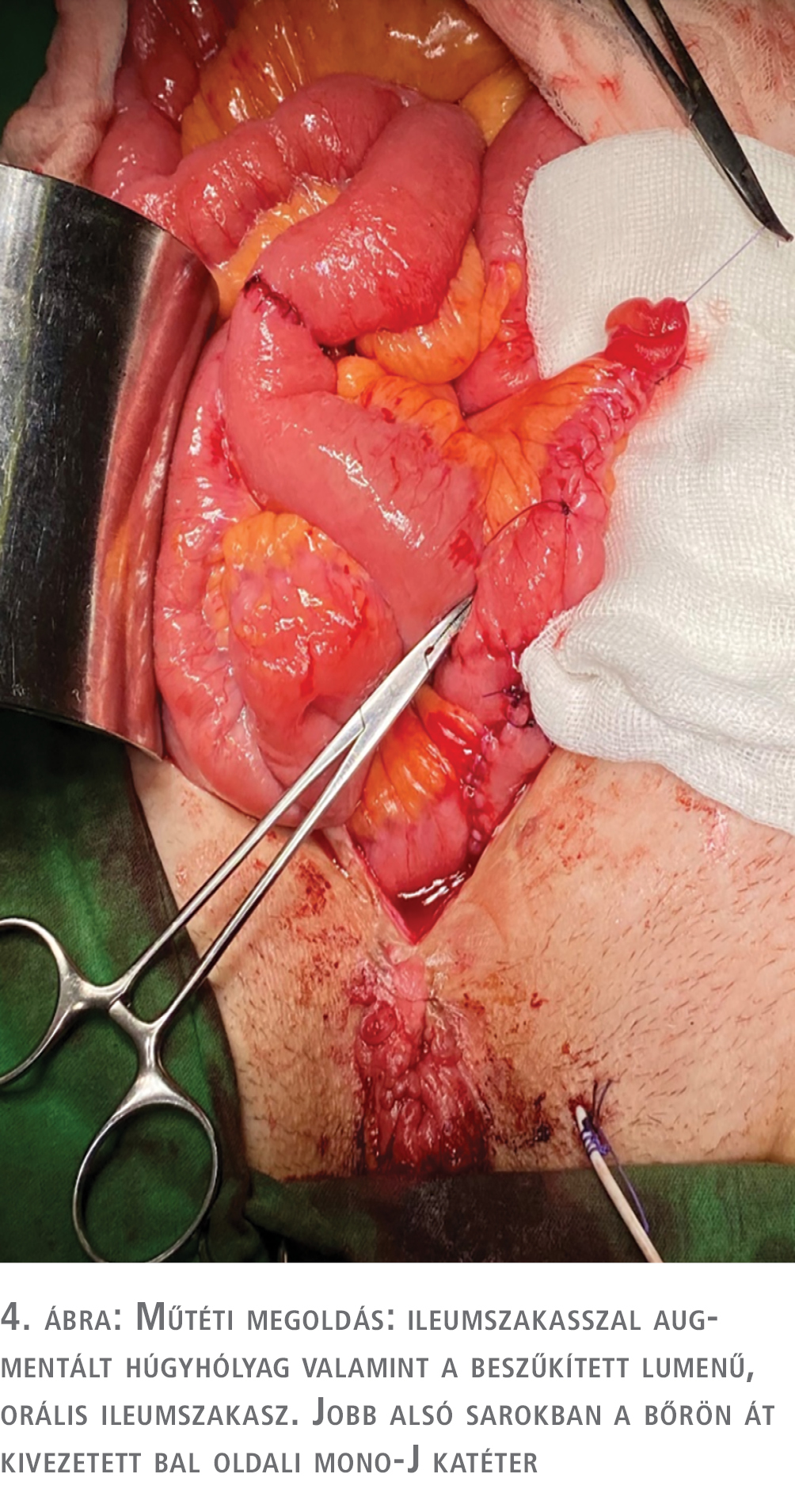
A húgyhólyag-bél anasztomózis tehermentesítésére a bal oldali szóló vesébe mono-J katétert, az augmentált húgyhólyagba a kialakított sztómán keresztül 12 Ch-s ballon katétert helyeztünk (5. ábra). A külső húgycsőnyílást két rétegben zártuk, a bél folytonosságát end-to-end anasztomózissal állítottunk helyre.
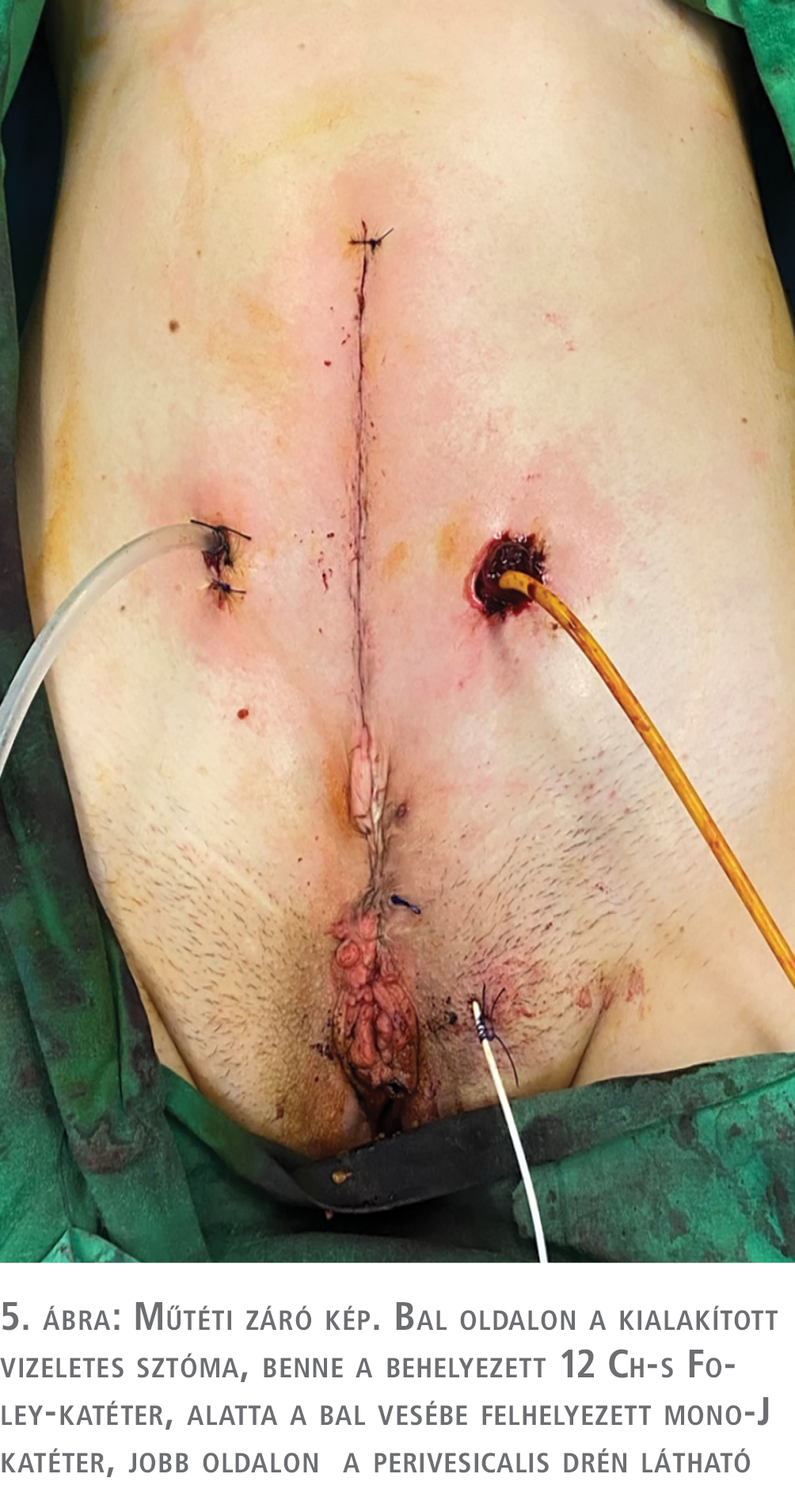
Műtét során, illetve a posztoperatív időszakban komplikációt nem észleltünk. Műtétet követő hatodik napon az augmentált húgyhólyag cisztográfiás vizsgálatát végeztük el. A felvételen jól ábrázolódott a kontinens sztóma, a normál tágasságú húgyhólyag, a bal uréter alsó szakaszáig terjedő passzív vesicoureteralis reflux valamint a bal vesébe felhelyezett mono-J katéter. A húgyhólyagból kontrasztanyag-kilépést nem észleltünk, sem a bél-húgyhólyag anasztomózis területén, sem a húgycső irányában (6. ábra). A beteget sztóma használatára megtanítva, pp. gyógyult sebbel, panaszmentesen bocsátottuk otthonába.
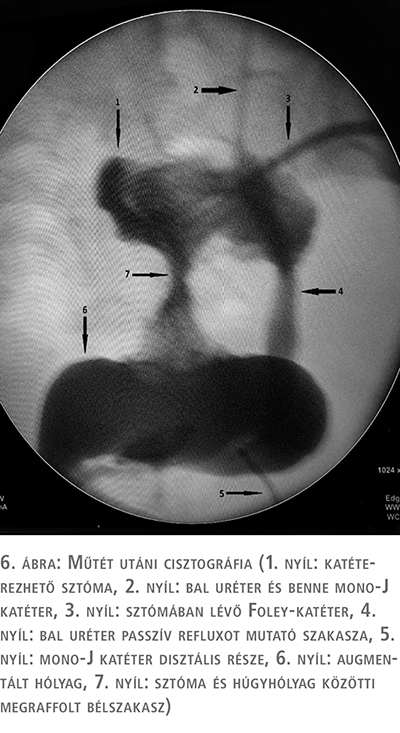
Kontrollvizsgálatok során a beteg kontinensnek bizonyult, sebgyógyulási zavart nem észleltünk. Naponta öt alkalommal végez önkatéterezést, húgyhólyagja 200-300 ml vizeletkapacitású. Jelenleg nőgyógyász-kollégák tervezik a beteg kettős hüvelyének helyreállító műtétjét, amely eredményeként coitusra alkalmas genitáliát hoznak létre.
Megbeszélés
A húgyhólyag-extrophia komplex fejlődési rendellenesség, amely gyakran más szervek érintettségével együtt jelentkezik. Fontos az állapot szülés utáni mielőbbi felismerése és a hólyag elsődleges zárása. A későbbiekben többnyire alsó húgyúti neurogén diszfunkció tünetei, eltérései alakulnak ki a betegnél, amelynek korai felismerése és korrekt kivizsgálása, ellátása megelőzheti a felső húgyúti károsodások, veseelégtelenség kialakulását.
A korrekciós műtétek tervezésekor a legfontosabb szempont, az alacsonynyomású, reziduummentes hólyagürülés biztosítása, amely lehetővé teszi a felső húgyutak funkciójának megőrzését és így az életveszélyes hosszú távú komplikációk megelőzését, másodlagos, de nagyon fontos kérdés a szociális kontinencia biztosítása, amely az életminőséget jelentősen javítja. Fiatal, jó compliance-szel rendelkező betegeknél a tartós eredmények és jobb életminőség eléréséhez, a katéterezhető sztómaképzéssel kialakított húgyhólyag-augmentáció biztosíthatja a legjobb megoldást. Az elvégzett húgyhólyag-augmentációk számáról megbízható hazai adatok sajnos nem állnak rendelkezésre. Az Egyesült Királyságban a 2000-es évek elején évente kb. 160 esetben végeztek ileumszakasszal húgyhólyag-augmentációt. A gasztrointesztinális traktus egyéb szakaszait (colon vagy coecum) kb. évi 20-20 esetben használták fel. 2010-es évekre mindez az ileum tekintetében évi kb. 90 esetre csökkent, míg a colon és coecum esetében lényegében nem változott. Nem úgy, mint az aspecifikus beavatkozások (különböző mesterséges hólyagdiverticulum-képzések) esetében. Ahol a 2000-es évek elején évi kb. 80 eset 2010-re gyakorlatilag 0-ra csökkent. Fenti adatokból is jól látszik, hogy a húgyhólyag-augmentációnak továbbra is létjogosultsága van megfelelő indikációk megléte esetén (5).
Bár fiatal nőbetegünk fő panaszát coitusra alkalmatlan genitáliája jelentette, részletes műtét előtti kivizsgálása kapcsán felismerésre került vizeletinkontineciája és neurogén alsó húgyúti rendellenessége. Esetünk is felhívja a figyelmet, hogy húgyhólyag-extrophia miatt korábban operált betegek urológiai szempontból rendszeres, életen át tartó követést, ellenőrzést igényelnek, így még időben felismerhetők és kezelhetők az életet veszélyeztető és az életminőséget rontó komplikációk is.
Következtetés
A húgyhólyag-extrophia miatt korábban hólyagzáráson átesett betegeknél gyakran észlelünk komplex, más szerveket is érintő fejlődési rendellenességeket, továbbá a hólyag primer zárása után ezen betegek rendszeres urológiai ellenőrzése szükséges a nagy eséllyel kialakuló neurogén alsó húgyúti diszfunkciók időben történő felismerése céljából. A jó időben végzett és a húgyhólyag tároló funkcióját javító, katéterezhető sztómaképzéssel kiegészített rekonstrukciós műtét alkalmas és eredményes hosszú távú megoldás ezen betegek további urológiai komplikációinak megelőzésére és életminőségének javítására.
Köszönetnyilvánítás
Ez úton is szeretnék köszönetet mondani dr. Keszthelyi Attila és dr. Majoros Attila docens uraknak az esteismertetés megírásban, lektorálásában nyújtott segítségért, támogatásért és tanácsokért. Külön köszönöm dr. Keszthelyi Attila docens úrnak a műtétnél való részvételem lehetőségét. Valamint köszönöm a Betegnek beleegyezését, amely nélkül nem jöhetett volna létre az eset tudományos célú bemutatása.
Irodalom
1. Chung A, Arianayagam M, Rashid P. Bacterial cystitis in women. Aust Fam Physician 2010; 39(5): 295–8.
2. Foxman B. Epidemiology of urinary tract infections: incidence, morbidity, and economic costs. Dis Mon 2003; 49(2): 53–70.
3. Simmering JE, et al. The Increase in Hospitalizations for Urinary Tract Infections and the Associated Costs in the United States 1998–2011. Open Forum Infect Dis 2017; 4(1): ofw281.
4. Verstraelen H, et al. The Vaginal Microbiome: I. Research Development, Lexicon, Defining “Normal” and the Dynamics Throughout Women’s Lives. J Low Genit Tract Dis, 2022; 26(1): 73–78.
5. Murta EF, Filho AC, Barcelos AC. Relation between vaginal and endocervical pH in pre- and post-menopausal women. Arch Gynecol Obstet 2005; 272(3): 211–3.
6. Paavonen JA, Brunham RC. Vaginitis in Nonpregnant Patients: ACOG Practice Bulletin Number 215. Obstet Gynecol 2020; 135(5): 1229–1230.
7. Czaja CA, et al. Population-based epidemiologic analysis of acute pyelonephritis. Clin Infect Dis 2007; 45(3): 273–80.
8. Yi-Te C, et al. Urinary tract infection pathogens and antimicrobial susceptibilities in Kobe, Japan and Taipei, Taiwan: an international analysis. J Int Med Res 2020; 48(2): 300060519867826.
9. Foxman B. Recurring urinary tract infection: incidence and risk factors. Am J Public Health 1990; 80(3): 331–3.
10. Foxman B, et al. Urinary tract infection among women aged 40 to 65: behavioral and sexual risk factors. J Clin Epidemiol 2001, 54(7): 710–8.
11. Hooton TM. Recurrent urinary tract infection in women. Int J Antimicrob Agents 2001; 17(4): 259–68.
12. Hooton TM, et al. Effect of Increased Daily Water Intake in Premenopausal Women With Recurrent Urinary Tract Infections: A Randomized Clinical Trial. JAMA Intern Med 2018; 178(11): 1509–1515.
13. Aziminia N, et al. Vaccines for the prevention of recurrent urinary tract infections: a systematic review. BJU Int 2019; 123(5): 753–768.
14. Beerepoot MA, et al. Nonantibiotic prophylaxis for recurrent urinary tract infections: a systematic review and meta-analysis of randomized controlled trials. J Urol 2013; 190(6): 1981–9.
15. Krauth BMA, Ács N, Békássy Sz, Nyirády P, Tenke P, Torzsa P. A Magyar Nőorvos Társaság és a Magyar Urológusok Társasága konszenzusdokumentuma a szövődménymentes cystitis kezeléséről. MAGYAR NŐORVOSOK LAPJA 2023; 86(18): X.
16. Bauer HW, et al. A long-term, multicenter, double-blind study of an Escherichia coli extract (OM-89) in female patients with recurrent urinary tract infections. Eur Urol 2005; 47(4): 542–8. discussion 548.
17. Cooper TE, et al. D-mannose for preventing and treating urinary tract infections. Cochrane Database Syst Rev 2022; 8(8): Cd013608.
18. Xia JY, et al. Consumption of cranberry as adjuvant therapy for urinary tract infections in susceptible populations: A systematic review and meta-analysis with trial sequential analysis. PLoS One 2021; 16(9): e0256992.
19. Harding C, et al. Methenamine hippurate compared with antibiotic prophylaxis to prevent recurrent urinary tract infections in women: the ALTAR non-inferiority RCT. Health Technol Assess 2022; 26(23): 1–172.
20. Goddard JC, Janssen DAW. Intravesical hyaluronic acid and chondroitin sulfate for recurrent urinary tract infections: systematic review and meta-analysis. Int Urogynecol J 2018; 29(7): 933–942.
21. Canales J, Rada G., Are probiotics effective in preventing urinary tract infection? Medwave 2018; 18(2): e7186.
22. Crandall CJ, et al. Breast cancer, endometrial cancer, and cardiovascular events in participants who used vaginal estrogen in the Women’s Health Initiative Observational Study. Menopause 2018; 25(1): 11–20.