Evaluation of prostate biopsies performed at Bajcsy-Zsilinszky Hospital, Hungary
DOI: 10.22591/magyurol.2019.4.monostoriz.134
Authors:
Monostori Zoltán dr., Szauer Orsolya dr., Böszörményi-Nagy Géza dr.
Bajcsy-Zsilinszky Kórház, Urológiai Osztály, Budapest (osztályvezető: Böszörményi-Nagy Géza dr.)
Summary
Introduction: In the year 2015 clinical data and results of 215 prostate biopsies were evaluated retrospectively.
Patient and method: We examined the pre-biopsy clinical data, the method of preparation, the circumstances of the intervention, and the results and complications. The relationship between complications and clinical data was investigated as well.
Results: The average of pre-sampling PSA values was 18,9 (2,2–817) ng/ml, with 37,7% of cases showing a tactile finding, suspicion of a tumour process. The average prostate size was found to be 54.3 ml. Of the samples taken, 102 were confirmed for prostate cancer (47,5%). There were 34 cases of complications with 13 cases of intervention.
Conclusion: The otherwise unified preparation was quite heterogeneous. Although antibiotics were given every time, its active ingredient, dose, and timing varied from one doctor to another. The accuracy of the biopsy the number and proportion of complications were acceptable compared to the literature. The physician-based individual evaluation of the assessment provides an opportunity for modifications to ensure uniform, standard conditions.
LAPSZÁM: MAGYAR UROLÓGIA | 2019 | 31. ÉVFOLYAM, 4. SZÁM
Összefoglalás
Bevezetés: A 2015-ös év folyamán, osztályunkon végzett 215 prosztatabiopszia adatait értékeltük.
Betegek és módszer: Vizsgáltuk a biopszia előtti klinikai adatokat, az előkészítés módját, a beavatkozás körülményeit, valamint az eredményeket és a szövődményeket. Vizsgáltuk továbbá a szövődmények és a klinikai adatok közötti összefüggéseket.
Eredmények: A mintavétel előtti PSA-értékek átlaga 18,9 (2,2–817) ng/ml volt, az esetek 37,7%-ában a tapintási lelet eltérést, tumoros folyamat gyanúját vetette fel. Az átlagos prosztataméretet 54,3 ml-nek találtuk. Az egyébként egységesnek gondolt előkészítés igencsak heterogénnek bizonyult. Bár antibiotikum adása minden alkalommal történt, annak hatóanyaga, dózisa, időpontja orvosonként eltérő volt. A végzett mintavételek közül 102 esetben igazolt a szövettani vizsgálat prosztatarákot (47,5%). Szövődményt 34 esetben észleltünk, beavatkozásra 13 esetben volt szükség.
Megbeszélés és következtetések: A találati pontosság az irodalmi adatokhoz hasonló. A szövődmények száma, aránya is összességében elfogadható. Az értékelés orvosra lebontott adatai alkalmat adnak módosításokra, egységes, standard körülmények biztosítására.
Bevezetés
A prosztatarák (PCa) a második leggyakrabban diagnosztizált ráktípus a férfiaknál a világon, az idősödő férfi populációban pedig a leggyakoribb a fejlett országokban.
A javuló egészségtudatosság, a megnövekedett prosztataspecifikus antigén (PSA) vizsgálatok száma, az egyes országokban bevezetett intézményesített szűrés és a biopsziás technikák javulása drámai emelkedést hoztak a PCa előfordulási gyakoriságában (1). A diagnózis standard eljárása jelenleg a transrectalis ultrahang- (TRUS) vezérelt prosztatabiopszia (2).
A képalkotó diagnosztikai módszerek megjelenése előtt a prosztatabiopsziát tapintás segítségével, a gát felől végezték el. A TRUS használata az 1970-es évek elején kezdődött az ultrahang megjelenésével. Az eredeti szextáns biopsziás eljárás összesen hat szövethenger mintavételét tartalmazta: a bázisról, a középső és az apex területéről kétoldalon (3). A 2000-es években megállapították, hogy a mintavételek számának megduplázása (6-ról 12-re) jelentősen növeli a prosztatarák kimutathatóságát anélkül, hogy emelkedne a biopszia utáni morbiditás (4). A 2019-ben hatályos irányelvek szerint 30 ml méretű prosztata esetén legalább 8, nagyobb prosztatánál 10-12 minta javasolt (5). A hatékonyság és a találati pontosság növelése céljából további igény mutatkozik a képvezérelt és célzottan végezhető biopsziák végzésére, úgymint irányított Doppler, valós idejű elasztográfia, ultrahangos kontrasztanyag használata, MRI-vezérelt és/vagy fúzionált mintavétel.
A prosztatabiopszia így folyamatosan változik, módszerei bővülnek. El kell végezni, ha a klinikai tünetek prosztatarákra utalnak. A döntésnek a korspecikfikus PSA-értéken, betegspecifikus kockázati tényezőkön, MR-vizsgálati eredményen, rectalis digitalis vizsgálaton (RDV), megelőző TURP-műtét szövettani leletén kell alapulnia.
Ismételt biopszia szükséges megelőző negatív biopszia esetén is, ha a PSA értéke emelkedő tendenciát mutat vagy tartósan emelkedett, valamint gyanús RDV, magasabb vizelet PCA3-szint és PI-RADS ³3 az MR-vizsgálati lelet esetén. Ugyancsak ismétlendő a mintavétel, ha a megelőző szövettani leletben ASAP (40% kockázat) vagy kiterjedt területen HGPIN (20-30% kockázat) mutatható ki (2). Alkalmazhatjuk a már felismert vagy kezelt betegség követésére (active surveillance, sugárkezelés utáni progresszió) is.
A nemzetközi tendenciák hazánkban is észlelhetőek. Magyarországon az elmúlt 6 évből rendelkezésre álló adatok alapján évente hozzávetőleg 6000 biopsziát végzünk, kórházunk urológiai osztályán átlagosan 200 beavatkozás történt (1. ábra) (6). Tanulmányunkban a 2015 év folyamán osztályunkon végzett 215 prosztatabiopszia adatait dolgoztuk fel.
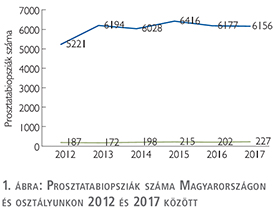
Vizsgáltuk a biopszia előtti klinikai adatokat, az előkészítés módját, a beavatkozás körülményeit, a kapott szövettani eredményeket és a szövődményeket. Vizsgáltuk továbbá a szövődmények és a klinikai adatok közötti összefüggéseket. Az értékelést saját céljainkra készítettük, de fontosnak tartjuk tanulságaink és eredményeink közzétételét.
Betegek és módszer
A 215 biopszián átesett beteg átlagéletkora 69,2 év, a mintavétel előtti PSA-értékek átlaga 18,9 (2,2–817) ng/ml volt, az átlagos prosztataméretet 54,3 ml-nek találtuk. Dysuriás panaszok 94 esetben jelentkeztek (43,7%) a biopsziát megelőző időszakban, ebből 59 esetben gyógyszeres kezelés indult (alfa-blokkoló 37 esetben, 5-alfa-reduktáz-gátló 19 esetben). Az esetek 37,7%-ában a tapintási lelet eltérést, tumoros folyamat gyanúját vetette fel. Az antibiotikum-profilaxist 1, 2 és 3 nappal a beavatkozás előtt kezdtük meg, leggyakrabban (66%) 2 nappal korábban.
Az antibiotikum hatóanyagában heterogenitás mutatkozott. Összesen 5 féle (ciprofloxacin, ofloxacin, levofloxacin, cefuroxim, metronidazol) került felírásra, amiből ciprofloxacin 43%-ban szerepelt. 38 beteg részesült vérhígító kezelésben, a beavatkozás előtt LMWH-ra átállítás történt.
A mintavételeket 2 készülékkel (Hitachi, 197, Brüel & Kjær 18 eset) végeztük.
A mintavételek számát a PSA-érték, a prosztatanagyság, illetve a beteg kuratív kezelésre való alkalmassága alapján határoztuk meg. Magas PSA-érték, ismert metasztatikus folyamat esetén kevesebb, már biopszián átesett, de emelkedő PSA-jú betegeknél, vagy korábbi ASAP, HG PIN esetén több mintát vettünk. Leggyakrabban, az esetek 77%-ában 12 mintás biopsziát végeztünk (2. ábra).
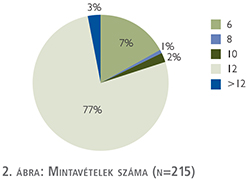
Eredmények
102 esetben igazolt a szövettani vizsgálat prosztatarákot (47,5%). Gleason-score szerinti megoszlásban: Gleason 3+3, 31%, Gleason 3+4, 37%, Gleason 4+3, 12%, Gleason 4+4, 4% és Gleason 4+5, 16%. 11 esetben HGPIN (5,1%), 8 esetben ASAP (3,7%), 102 esetben BPH (47,5%), 40 esetben prostatitis chronica (18,6%) volt a szövettani vélemény.
Vizsgáltuk a tapintási lelet összefüggését a szövettani eredménnyel. Míg összes betegünknél 37,7%-ban, igazolt prosztatakarcinóma esetén 52%-ban, a negatív esetekben 25%-ban volt pozitív a tapintási lelet.
Szövődményt 34 esetben észleltünk (16%), amelyből beavatkozásra (rectum tamponálás, katéterezés, kórházi felvétel, antibiotikum adása lázas állapot miatt) 13 esetben volt szükség (6%). Ellátásra szoruló rectalis vérzés (tamponálás) 3 esetben (1,3%) fordult elő (3. ábra).
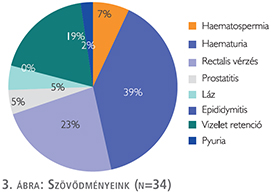
A 38 korábban vérhígító kezelést kapott betegnél 26%-ban, míg a vérhígítót korábban nem kapó esetekben 14%-ban észleltünk szövődményt.
Az antibiotikum-profilaxis szempontjából vizsgálva a szövődmények arányát megállapítható, hogy nincs jelentős különbség a különböző antibiotikumok között (4. ábra).
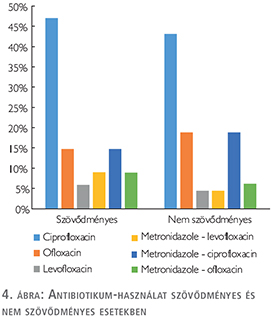
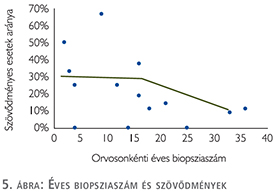
Összefüggést találtunk viszont az orvosonkénti beavatkozások száma és a szövődmények előfordulása között. Évi 17 fölötti esetszám esetén tapasztalható a szövődmények számának a csökkenése (5. ábra).
Megbeszélés és következtetések
A mintavételeink során észlelt 47,5%-os találati arány megfelel más centrumok adatainak (7).
Vizsgálataink alapján a rectalis digitalis igazolt prosztatarák esetén alig több mint az esetek felében jelzett eltérést. Negatív biopszia esetén azonban a pozitív tapintási lelet az ismételt mintavétel indikációját erősítheti.
A vizsgálat rámutatott, hogy az egyébként egységesnek gondolt előkészítés igencsak heterogénnek bizonyult. Bár antibiotikum adása minden alkalommal történt, annak hatóanyaga, dózisa, időpontja orvosonként eltérő volt.
Az antikoagulált betegeknél gyakrabban találtunk szövődményt.
Az értékelés orvosra lebontott adatai alkalmat adnak egyéni módosításokra, egységes, standard körülmények biztosítására.
Jelenleg a mintavételeket egységes előkészítéssel (Monural), előzetes, standardizált leletezésű MR-vizsgálatot követően, azaz célzottan végezzük. Későbbiekben tervezzük az így végzett mintavételek feldolgozását.
References
1. Ferlay J, et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer 2015; 136: E359. https://doi.org/10.1002/ijc.29210
2. Shahrokh F Shariat, Claus G Roehrborn. Using Biopsy to Detect Prostate Cancer FACS. Rev Urol 2008 Fall; 10(4): 262–280.
3. Hodge KK, McNeal JE, Terris MK, Stamey TA. Random systematic versus directed ultrasound guided transrectal core biopsies of the prostate. J Urol 1989; 142: 71–74. https://doi.org/10.1016/S0022-5347(17)38663-9
4. Eichler K, Hempel S, Wilby J, Myers L, Bachmann LM, Kleijnen J. Diagnostic value of systematic biopsy methods in the investigation of prostate cancer: a systematic review. J Urol 2006; 175: 1605–1612. https://doi.org/10.1016/S0022-5347(05)00957-2
5. EAU Guidelines Prostate Cancer 5.2. ( https://uroweb.org/guideline/prostate-cancer/#note_154)
6. Böszörményi-Nagy G. Beszámoló az urológiai fekvőbeteg-ellátásról a 2015-ös adatok alapján. MAGYAR UROLÓGIA 2017; 29(1).
7. Mottet N, Bastian PJ, Bellmunt J, van den Bergh RCN, Bolla M, van Casteren NJ, et al. Guidelines on Prostate Cancer. Eur Assoc Urol 2014.