Re-evaluation of prostate biopsies at our hospital
DOI: 10.22591/magyurol.2022.4.balogha.152
Authors:
Balogh Ákos dr., Monostori Zoltán dr., Böszörményi-Nagy Géza dr.
Bajcsy-Zsilinszky Kórház, Urológiai Osztály, Budapest
(osztályvezető: Böszörményi-Nagy Géza dr.)
Summary
Introduction: Our work is a continuation of a study conducted in 2015 at the Urology Department of the Bajcsy-Zsilinszky Hospital and Outpatient Clinic.
Patients and methods: We studied clinical data before the prostate biopsy, method of preparation, conditions of intervention, the results and complications. We also examined the relationships between complications and clinical data.
Results: The overall mean PSA values before histological sampling were found to be 58.65 ng/ml, while excluding values above 100 ng/ml being found to be 15.97 ng/ml. The mean age of the patients was 71.9 years.
In 15.65% of the cases, DRE showed a discrepancy that suggested a tumour process. In cases of histologically proven carcinomas, the rate of positive DRE was 78% and 22% in the case of a negative histological result.
The type of antibiotic prophylaxis was changed (fosfomycin in 76%). In this group of patients, the incidence of febrile complications was found to be 1.17%.
Conclusions: The introduction of standardized antibiotic prophylaxis has reduced the incidence of infectious complications.
Our results are comparable with the literature data the predictability of DRE, the hit rate and the incidence of infectious complications show a more favourable picture.
LAPSZÁM: MAGYAR UROLÓGIA | 2022 | 34. ÉVFOLYAM, 4. SZÁM
Összefoglalás
Bevezetés: Munkánk az osztályunkon 2015-ben végzett tanulmány folytatása, az azóta megváltozott antibiotikumprofilaxis hatékonyságának értékelése.
Betegek és módszer: Vizsgáltuk a prosztatabiopszia előtti klinikai adatokat, az előkészítés módját, a beavatkozás körülményeit, valamint az eredményeket és a szövődményeket. Vizsgáltuk továbbá a szövődmények és a klinikai adatok közötti összefüggéseket.
Eredmények: A szövettani mintavétel előtti PSA-értékek teljes átlagát 58,65 ng/ml-nek, csak a 100 ng/ml alatti értékeket nézve 15,97 ng/ml-nek találtuk. A betegek átlagéletkora 71,9 év volt.
Az esetek 15,65%-ában mutatott a tapintási lelet olyan eltérést, amely tumoros folyamat gyanúját vetette fel. Későbbiekben szövettanilag igazolt prosztatakarcinóma esetén 78%-ban, míg negatív szövettani eredmény esetén 22%-ban volt pozitív a tapintási lelet.
Törekedtünk az egységes antibiotikumprofilaxisra (76%-ban fosfomycin). A lázas szövődmények előfordulási gyakoriságát 1,17%-nak találtuk.
Megbeszélés: Eredményeinket az irodalmi adatokkal összevetve, a tapintási lelet prediktivitása, a találati arány, a fertőzéses szövődmények előfordulása az irodalmi adatoknál kedvezőbb képet mutatnak.
Az egységesített antibiotikumprofilaxis bevezetése csökkentette a fertőzéses szövődmények előfordulását.
Bevezetés
Világszerte férfiak esetében a prosztatadaganat a második leggyakrabban diagnosztizált daganattípus és a rákos halálozás tekintetében ötödik helyen van a 2020-as adatok szerint. Az incidencia aránya háromszor magasabb a fejlett országokban, míg a mortalitási arányok nem mutatnak ilyen különbséget (1).
A prosztatakarcinóma diagnosztikájában az utóbbi években jelentős változások történtek. A képalkotó módszerek fejlődése, a prosztataspecifikus-antigén (PSA) vizsgálatának széles körű elterjedése a korai felismerést megkönnyítette, ugyanakkor a transrectalis ultrahanggal (TRUS) vezérelt prosztatabiopszia a prosztatakarcinóma diagnosztikájának még mindig a standard módszere.
Ha a beavatkozással járó szövődményeket vizsgáljuk, azt tapasztalhatjuk, hogy az elmúlt évtizedben a prosztatabiopszia utáni fertőzéses szövődmények az irodalmi adatok szerint megnövekedtek (2). A transrectalis prosztatabiposziát követően jelentkező fertőzések gyakori oka a fluorokinolonok-rezisztens E. Coli (3). A profilaktikus antimikrobiális szerek alkalmazása a TRUS-biopsziánál több tanulmány szerint is csökkenti a beavatkozás utáni lázas állapotot és a húgyúti fertőzést (4). Ezen irodalmi adatok alapján, osztályunkon felhagytunk a fluorokinolonok profilaktikus alkalmazásával TRUS-biopszia előtt és egységesen fosfomycin terápiában részesítettük a betegeket.
Kutatásunk egyik célja a korábbi vizsgálatunkban leírt, heterogén antibiotikumprofilaxist felváltó, új paradigma igazolása.
Munkánk egy előző kutatáson alapul (5), amelyben a 2015-ös év folyamán a Bajcsy-Zsilinszky Kórház és Rendelőintézet Urológiai Osztályán végzett prosztatabiopsziák adatait dolgoztuk fel. A vizsgálatban áttekintettük a biopszia előtti klinikai adatokat, az előkészítés módját, beavatkozás körülményeit, a kapott szövettani eredményeket és a szövődményeket. Vizsgáltuk továbbá a szövődmények és a klinikai adatok közötti összefüggéseket.
A 2015-ös évi kutatás folytatásaként jelen dolgozatban beszámolunk a Bajcsy-Zsilinszky Kórház Urológiai Osztályán 2020–21-es években végzett prosztatabiopsziákról. 2015-ben 215 beteg adatait vettük alapul, míg a jelen kutatásban 230 beteg vett részt.
Betegek és módszerek
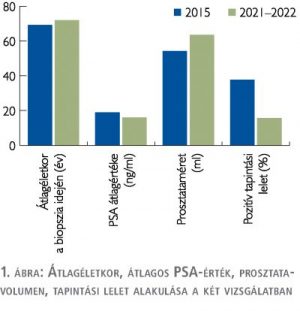
A 230 biopszián átesett betegek átlagéletkora 71,9 év, az előző vizsgálathoz képest (69,2 év) enyhén magasabb.
A szövettani mintavétel előtti PSA-értékek teljes átlagát 58,65 ng/ml-nek, csak a 100 ng/ml alatti értékeket nézve 15,97 ng/ml-nek találtuk, amíg a 2015-ös év PSA átlaga: 18,9 ng/ml volt.
Az átlagos prosztataméret: 63,55 ml (2015-ben 54,3 ml) volt.
Az esetek 15,65%-ában mutatott a tapintási lelet olyan eltérést, amely tumoros folyamat gyanúját vetette fel (36/230) (2015-ben ez az arány 37,7% volt) (1. ábra).
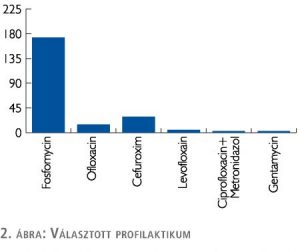
A korábbi vizsgálatban jelentős heterogenitás mutatkozott a választott profilaktikum hatóanyagában. Összesen 5 féle antibiotikum (ciprofloxacin, ofloxacin, levofloxacin, cefuroxim, metronidazol) került felírásra, amiből ciprofloxacin 43%-ban szerepelt. Legtöbb esetben (az esetek 96%-ában) valamilyen kinolonszármazék került felírásra.
A fentieknek megfelelően homogenizáltabb antibiotikumprofilaxist alkalmaztunk: leggyakoribb profilaktikus készítmény a fosfomycin lett (175/230), ezen kívül cefuroxim (29/230), ofloxacin (15/230) volt a legtöbbször alkalmazva. Előfordult még 5 esetben levofloxacin, 3-3 esetben ciprofloxacin + metronidazol, illetve gentamycin alkalmazása (2. ábra).
Véralvadásgátló-kezelésben a biopszián átesettek 7,4%-a részesült (17/230).
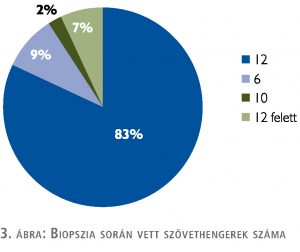
A mintavételek számát a PSA-érték, a prosztata volumene, MR-vizsgálati eredmény határozta meg. Jelentősen megemelkedett PSA-értéknél, igazolt metasztázis esetén kevesebb; ismételt, korábban negatív biopsziás eredményt követően emelkedő PSA-érték, illetve korábbi szövettani eredményben igazolt High Grade PIN, ASAP esetén megnöveltük a szövethengerek számát.
Az esetek 83%-ában történt 12 minta vétele (3. ábra).
Eredmények
Összesen 131 esetben igazolt a szövettani vizsgálat prosztatakarcinómát (56,9%). Ugyanezen adat 2015-ben 47,5% volt. Gleason-score szerinti megosztásban: 3+3: 15,2% (35/230), 3+4: 9,56% (22/230), 3+5: 1,79% (4/230), 4+3: 7,39% (17/230), 4+4: 7,82% (18/230), 4+5: 10% (23/230), 5+3: 1,3% (3/230), 5+4: 1,74% (4/230), 5+5: 2,17% (5/230) volt (4. ábra).
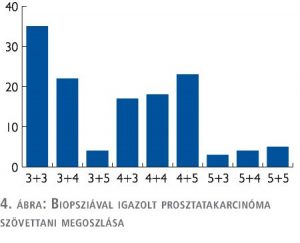
Krónikus limfoid leukémia 1 esetben került igazolásra. HGPIN 5,65% (13/230), ASAP 1,3% (3/230) került felismerésre.
Az igazolt prosztatakarcinómák szövettani megoszlása a 2015-ös vizsgálatban tapasztaltakkal összemérhető. 133 esetben daganat igazolódott (57,8%), míg a 2015-ös vizsgálatban ez az arány csupán 47,5%.
Megvizsgáltuk a tapintási lelet prediktív értékét. Az összes betegünk esetén 15,65%-ban, a későbbiekben szövettanilag igazolt prosztatakarcinóma esetén 78%-ban, míg negatív szövettani eredmény esetén 22%-ban volt pozitív a tapintási lelet. Ezek az adatok szintén összevethetők korábbi eredményeinkkel. (2015-ben: összes beteg esetén 37,7%-ban volt pozitív tapintási lelet, igazolt prosztatakarcinóma esetén 52%-ban, a negatív esetekben 25%-ban volt pozitív).
Szövődményt 11 esetben észleltünk (5%). Ez jóval az irodalmi átlag és a 2015-ös adataink alatt található (16%) (6). Leggyakoribb a vérzéses szövődmény volt, ez 8 esetben fordult elő. Lázas állapot 6 esetben, retenció 2 esetben szerepelt. Néhány betegnél többfajta szövődmény is előfordult.
A fosfomycin profilaxisban részesült betegek közül 2 esetben fordult elő lázas szövődmény (1,17%). 2015-ben a kinolonokkal kezelt betegek csoportjában ez az arány 1,86% volt. (egyedül itt van megemlítve, hogy a 2015-ös vizsgálatban mi volt a domináló antibiotikum) (5. ábra).
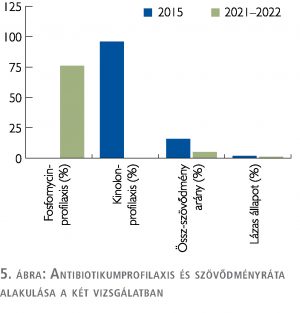
Megbeszélés
A mintavételeink során észlelt 57,8%-os találati arány az irodalmi adatokhoz képest jóval kedvezőbb (7) és jelentős javulást mutat a 2015-ös adatokhoz képest is.
Vizsgálataink alapján a pozitív rektális digitális lelet 78%-ban szövettanilag is igazolt prosztatakarcinómát mutatott. Ez az eredmény a nemzetközi adatoknál magasabb arány (8).
Azoknál a betegnél, ahol pozitív tapintási lelet mellé negatív hisztológia társult, további megfigyelést tartottunk szükségesnek.
Jelen kutatásunk alapján levonható az a következtetés, hogy a megváltoztatott antibiotikumprofilaxis, amelyet az osztályunkon 2 éve használunk, kedvezően befolyásolta a fertőzéses szövődmények előfordulási gyakoriságát.
Irodalom
1. Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021; 71(3): 209–249.
https://doi.org/10.3322/caac.21660
2. Nam RK, Saskin R, Lee Y, et al. Increasing hospital admission rates for urological complications after transrectal ultrasound guided prostate biopsy. J Urol 2010; 183(3): 963–968.
https://doi.org/10.1016/j.juro.2009.11.043
3. Liss MA, Johnson JR, Porter SB, et al. Clinical and microbiological determinants of infection after transrectal prostate biopsy. Clin Infect Dis 2015; 60(7): 979–987.
https://doi.org/10.1093/cid/ciu1129
4. Melekos MD. Efficacy of prophylactic antimicrobial regimens in preventing infectious complications after transrectal biopsy of the prostate. Int Urol Nephrol 1990; 22(3): 257–62.
https://doi.org/10.1007/BF02550403. PMID: 2210982
5. Monostori, et al. Prosztatabiopsziáink értékelése. Magy Urol 2019; 31(4): 134–136. https://doi:10.22591/magyurol.2019.4.monostoriz.134
6. Loeb S, Vellekoop A, Ahmed HU, et al. Systematic review of complications of prostate biopsy. Eur Urol 2013; 64(6): 876–892.
https://doi.org/10.1016/j.eururo.2013.05.049
7. Ahmed HU, El-Shater Bosaily A, Brown LC, et al. Diagnostic accuracy of multi-parametric MRI and TRUS biopsy in prostate cancer (PROMIS): a paired validating confirmatory study. Lancet 2017; 389(10071): 815–822.
https://doi.org/10.1016/S0140-6736(16)32401-1
8. Naji L, Randhawa H, Sohani Z, et al. Digital rectal examination for prostate cancer screening in primary care: a systematic review and meta-analysis. Ann Fam Med 2018; 16(2): 149–154.
https://doi.org/10.1370/afm.2205